LIMSwiki
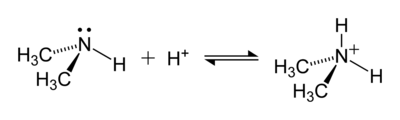
Ammoniumioni on moniatominen positiviinen kompleksi-ioni, jonka kemiallinen kaava on NH4+. Se syntyy ammoniakkimolekyylin (NH3) ottaessa vastaan protonin eli vetyionin (H+).
Ammoniumioni esiintyy kationina ammoniumsuoloissa, kuten ammoniumkloridissa eli salmiakissa. Ammoniumsuolat muistuttavat ominaisuuksiltaan huomattavasti vastaavia alkalimetallien suoloja, ja niinpä ammoniumionia kutsutaankin pseudoalkalimetalli-ioniksi. Lisäksi ammoniumioneja esiintyy jonkin verran myös ammoniakin vesiliuoksessa, sillä ammoniakki on emäs, jonka molekyyli voi ottaa vesimolekyyliltä vastaan protonin muodostaen ammoniumionin.
Nimeä ammonium käytetään myös kationeista, jotka syntyvät jonkin amiinin ottaessa vastaan protonin, sekä kvaternäärisissä ammoniumyhdisteissä esiintyvistä ioneista NR4+. Näiden voidaan ajatella syntyvän ammoniumionista (NH4+ korvaamalla yksi tai useampi siinä olevista vetyatomeista jollakin orgaanisella radikaalilla, josta käytetään merkintää R.
Happo- ja emäsominaisuudet

Ammoniumioni syntyy, kun ammoniakki, joka on heikko emäs, reagoi jonkin hapon kanssa vastaanottaen protonin:
- H+ + NH3 → NH4+
Ammoniumioni itse on heikko happo, jonka happovakio (pKa) on 9,2.[1] Happoluonteensa vuoksi se reagoi Brønstedin happo-emästeorian mukaisesti emästen kanssa muodostaen ammoniakkia:
- NH4+ + B- HB + NH3
Tämän vuoksi ammoniakkia syntyy ammoniumsuolojen väkevien liuosten reagoidessa vahvojen emästen kanssa. Toisaalta kun ammoniakki liukenee veteen, pieni osa siitä muuttuu ammoniumioneiksi:
- H3O+ + NH3 H2O + NH4+
Kuinka suuri osa ammoniakista muuttuu ammoniumioneiksi, riippuu liuoksen pH:sta. Jos pH on alhainen eli liuos on hapan, reaktion tasapaino siirtyy oikealle: suurempi määrä ammoniakkimolekyylejä muuttuu ammoniumioneiksi. Jos pH on korkea eli liuos on emäksinen, tasapaino siirtyy vasemmalle, sillä hydroksidi-ionit ottavat protoneja ammoniumioneilta, jotka muuttuvat takaisin ammoniakiksi.
Ammoniumyhdisteitä voi syntyä myös höyrytilassa. Esimerkiksi, jos ammoniakkihöyry joutuu kosketuksiin vetykloridihöyryn kanssa, syntyy valkoinen, ammoniumkloridista koostuva pilvi, joka vähitellen tiivistyy kiinteänä aineena ohueksi kerrostumaksi lähellä olevien kappaleiden pinnoille.
Ammoniumsuolat

Ammonium esiintyy kationina monissa suoloissa kuten ammoniumkarbonaatissa, ammoniumkloridissa ja ammoniumnitraatissa. Useimmat yksinkertaiset ammoniumsuolat liukenevat runsaasti veteen. Poikkeuksena on ammoniumheksakloroplatinaatti, jota on aikoinaan käytetty ammoniumin tutkimukseen. Ammoniumnitraatti ja varsinkin ammoniumperkloraatti ovat herkästi räjähtäviä, ja niissä ammoniumioni toimii pelkistimenä.
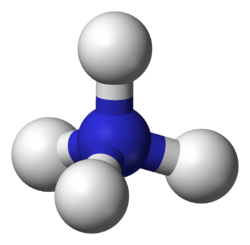
Rakenne ja sidokset
Ammoniakin typpiatomilla (N) on vapaa elektronipari, jolla se voi sitoa protonin (H+). Tämän vuoksi ammoniumionissa kaikki neljä N-H -sidosta ovat samanlaisia, polaarisia kovalenttisia sidoksia. Ioni on isoelektrinen metaanin ja boorihydridin kanssa. Ammoniumionin läpimitta on 175 pm, mikä on lähellä cesiumionin läpimittaa, 183 pm.
Orgaaniset ammoniumionit
- Katso myös: amiini
Ammoniumionin vetyatomit voidaan korvata alkyylilla tai muulla orgaanisella ryhmällä, jolloin saadaan substituoituja ammoniumioneja eli IUPACin nimistön mukaan aminium-ioneja. Orgaanisten ryhmien lukumäärästä riippuen näitä ioneja sanotaan primaarisiksi, sekundaarisiksi, tertiaarisiksi tai kvaternäärisiksi ammoniumkationeiksi. Kvaternäärisiä ammoniumioneja lukuun ottamatta ne ovat heikkoja happoja.
Esimerkkinä reaktiosta, jossa syntyy tällainen ioni, voidaan mainita dimetyyliamiinin (CH3)2NH ja happojen väliset reaktiot, joissa syntyy dimetyyliammonium-ioni (CH3)2NH2+:
Kvaternäärisissä ammoniumioneissa on typpiatomiin sitoutuneina neljä orgaanista ryhmää. Niissä ei ole typpiatomiin sitoutunutta vetyatomia. Näitä kationeja, esimerkiksi tetra-n-butyyliammoniumia, käytetään joskus korvaamaan natrium- tai kaliumionit vastaavan anionin liukoisuuden nostamiseksi orgaanisissa liuottimissa. Primaariset, sekundaariset ja tertiaariset ammoniumsuolat vaikuttavat samoin, mutta ovat vähemmän lipofiilisiä. Niitä käytetään myös faasimuutoskatalysaattoreina ja tensideinä.
Biologinen merkitys
Ammoniumioneja syntyy eläinten aineenvaihdunnan jäteaineina. Kaloista ja selkärangattomista vesieläimistä se erittyy suoraan veteen. Nisäkkäillä, hailla ja sammakkoeläimillä se muuttuu ureasyklissä ureaksi, koska on vähemmän myrkyllistä ja tehokkaammin varastoitavaa. Lintujen, matelijoiden ja maan matojen aineenvaihdunnassa syntyvä ammonium muuttuu virtsahapoksi, joka on kiinteää ja voidaan sen vuoksi erittää menettämättä paljonkaan vettä.[2]
Ammonium on tärkeä typen lähde monille kasveille, varsinkin niille, jotka kasvavat vähähappisessa maaperäksi. Lannoitteina käytetäänkin muun muassa ammoniumnitraattia ja ammoniumsulfaattia.[3] Liian suurena määränä ammonium on kuitenkin useimmille lajeille myrkyllistä, ja sen vuoksi sitä harvoin käytetään kasvien ainoana typen lähteenä.[4]
Metallinen ammonium
Ammoniumionilla on hyvin samankaltaisia ominaisuuksia kuin raskaimmilla alkalimetalleilla, ja sitä pidetään usein niiden läheisenä sukulaisena.[5][6][7] Tämän vuoksi oletetaankin, että hyvin suuressa paineessa ammonium voi esiintyä metallisessa muodossa, jolloin ammoniumionit muodostaisivat kidehilan ja niiden välissä esiintyisi vapaiden elektronien meri samaan tapaan kuin metalleissa. Metallista ammoniumia on arveltu esiintyvän suurten kaasuplaneetojen kuten Uranuksen ja Neptunuksen sisuksissa.[6][7]
Vaikka puhdasta metallista ammoniumia ei ole voitu valmistaa, ammonium voi monien metallien tavoin muodostaa elohopean kanssa tahdasmaisen seoksen, ammoniumamalgaamin, jota saadaan elektrolysoimalla ammoniumkloridia elohopean toimiessa katodina. Tämä amalgaami on kuitenkin pysymätön, sillä siinä oleva ammonium hajoaa vähitellen ammoniakiksi ja vedyksi.[8]
Lähteet
- Lahti, Kimmo & Rönkä, Antti: Biologia: Ympäristöekologia. Helsinki: WSOY oppimateriaalit, 2006. ISBN 951-0-29702-X
Viitteet
- ↑ Antti Kivinen, Osmo Mäkitie: Kemia, s. 195. Otava, 1988. ISBN 951-1-10136-6
- ↑ Neil A. Campbell, Jane B. Reece: Biology, 5. painos, s. 937–938. San Francisco: Pearson Education inc., 2002. ISBN 0-8053-6624-5
- ↑ Otavan iso Fokus, 1. osa (A–El), s. 156, art. Ammonium. Otava, 1973. ISBN 951-1-00273-3
- ↑ D. R. Britto & H. J. Kronzucker: NH4+ toxicity in higher plants: a critical review. Journal of Plant Physiology, 2002, nro 159. doi:10.1078/0176-1617-0774 Artikkelin verkkoversio.
- ↑ A. F. Holleman & E. Wiberg: Inorganic Chemistry. San Diego: Academic Press, 2001. ISBN ISBN 0-12-352651-5
- ↑ a b D. J. Stevenson: Does metallic ammonium exist?. Nature, 1975, nro 257. doi:10.1038/258222a0 Artikkelin verkkoversio.
- ↑ a b M. J. M. Bernal, H. S. W. Massey: Metallic Ammonium. Monthly Notices of the Royal Astronomical Society, 1954, nro 114. Wiley-Blackwell. Bibcode:1954MNRAS.114..172B Artikkelin verkkoversio.
- ↑ Facta 2001, s. 460, art. Ammonium. WSOY, 1981. ISBN 951-0-10222-9