Clinfowiki
Sommaire
Bryobiotina
| Règne | Plantae |
|---|



Les bryophytes sont des plantes terrestres thalloïdes ou feuillées non vascularisées. Parmi les plantes actuelles, les bryophytes terrestres et les bryophytes aquatiques sont celles qui ont conservé le plus de caractères des premières plantes ayant colonisé la terre ferme. Les ancêtres de toutes les plantes terrestres, donc des bryophytes, sont des algues vertes, Charophyceae.
Même si certaines structures anatomiques leur permettent de résister à la dessiccation, les Bryophytes sont encore extrêmement dépendantes de l'eau ou des milieux humides, ou en tout cas d'une hygrométrie minimale au moment de leur reproduction. Cette exigence n'empêche pas une grande plasticité écologique qui leur permet de vivre dans toutes les régions du globe, de l'équateur jusqu'aux pôles[4].
Pris au sens large, c'est-à-dire celui des classifications traditionnelles, le terme « bryophyte » s'applique aux trois embranchements de plantes terrestres qui ne possèdent pas de vrai système vasculaire : les Marchantiophyta (hépatiques), les Bryophyta s.s. (mousses, sphaignes) et les Anthocerotophyta (anthocérotes), regroupés dans le sous-règne des Bryobiotina du règne des Chlorobiota[5],[6]. Au sens strict de la botanique, l'embranchement des Bryophyta ne concerne donc que les mousses et les sphaignes (à l'exception donc des Marchantiophyta et des Anthocerotophyta).
Avec près de 25 000 espèces de mousses et sphaignes, 9 000 espèces d'hépatiques (Marchantiophyta) et 300 espèces d'anthocérotes, les bryophytes constituent le second groupe de végétaux terrestres, après les Dicotylédones.
Composants importants des biotopes forestiers et montagnards, les bryophytes sont une source majeure de la biodiversité spécifique des environnements frais ou humides et contribuent de façon non négligeable à la structure et au fonctionnement des écosystèmes que ce soit en termes de dynamique écologique, de formation des sols et plus largement dans les cycles biogéochimiques et la régulation des climats[4].
Historique

Connues et utilisées depuis la nuit des temps, les bryophytes ne font l'objet d'une attention particulière que depuis la fin du XVIIIe siècle, le seul ouvrage consacré exclusivement aux mousses avant étant l'Historia muscorum de Johann Jacob Dillenius publié en 1741[7]. Au cours des siècles précédents, les bryophytes, comme les autres cryptogames (taxon désormais non valide comprenant les algues, les lichens, les fougères), sont en effet peu étudiées compte tenu de leur petitesse, de leur organe reproducteur non visible et du peu d'avantages que l'Homme arrive à en tirer[8]. En 1784, Johannes Hedwig, « père de la bryologie », en fait un ensemble véritablement naturel, subdivisé en Musci frondosi (Mousses) et Musci hepatici (Hépatiques)[9]. En 1789, Jussieu propose une classification naturelle dans son Genera plantarum et est le premier à utiliser le terme de mousse pour représenter cet ensemble qu'il classe dans les « plantes sans fleurs » avec les Fungi (champignons), Algae (algues) et Filices (fougères)[8]. Le terme Bryophyte est inventé en 1864 par le botaniste allemand Alexander Braun qui accole deux mots grecs, bryo (« mousse ») et phytos (« plante »)[10].
Les classifications phylogénétiques récentes intègrent les bryophytes dans le taxon monophylétique des Embryophytes, plantes terrestres comprenant les « cryptogames » (Bryophytes et Ptéridophytes)[8]. La systématique phylogénétique suggère également qu'elles sont un groupe paraphylétique (la monophylie ou la polyphylie de ce taxon a longtemps été discutée[11]), abandonné par les cladistes mais conservé comme grade évolutif par les systématiciens évolutionnistes. Il comporte trois phylums : les Marchantiophytes (hépatiques), les Bryophytes s.s. (mousse, sphaigne) et les Anthocérotophytes (anthocérotes)[12].
Cycle de vie
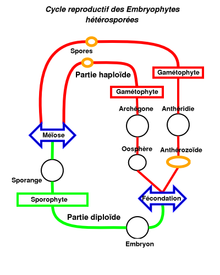






Comme pour les algues vertes et les plantes vertes, le cycle de vie présente une alternance de sporophytes (ou sporogone) et de gamétophytes, mais, comme pour toutes les Embryophytes, les anthérozoïdes (ou spermatozoïdes) sont protégés (et formés) par des anthéridies et les oosphères par des archégones (caractères partagés avec les plantes vasculaires). Les mousses forment souvent, au sommet de leur axe, une couronne de feuilles plus grandes, appelée soit anthéridiophore soit archégoniophore, qui porte à leur sommet les structures fertiles (anthéridies et archégones) en forme de corbeilles qui renferment ainsi les gamétanges. Dans ces organes sexuels, les gamétanges sont généralement séparés par des poils stériles (appelés paraphyses) qui jouent un rôle protecteur contre la dessiccation en favorisant la rétention d'eau par capillarité[13].
La fécondation est une zoïdogamie aquatique (oogamie), les anthérozoïdes (ou spermatozoïdes) ciliés, libérés de l'anthéridie par gélification et rupture de la paroi, sont entraînés par les gouttes d'eau de pluie ou de rosée, retenue par les feuilles ou les thalles (ou par les éclaboussures de gouttes de pluie lorsque les mousses sont dioïques) dans lesquelles ils se déplacent pour atteindre l'oosphère (la distance maximale de dispersion des spermatozoïdes étant d'une dizaine de centimètres)[14]. L'embryon qui en résulte est nourri et protégé par le gamétophyte (matrotrophie). Le sporophyte non ramifié fixé sur le gamétophyte ne devient jamais indépendant de celui-ci. Le gamétophyte haploïde est donc le stade dominant sous lequel se rencontre la plante alors que le sporophyte est éphémère. Il peut être monoïque (plante bisexuée) ou dioïque (plante monosexuée). Lorsqu'il est monoïque, une protandrie (maturation de l'anthéridie avancée par rapport à celle de l'archégone) permet généralement d'éviter l'autofécondation[15].
Les spores sont entourées d'une paroi contenant de la sporopollénine qui les protège de la dessiccation au cours de la dissémination[16]. Les botanistes parlent de cycle digénétique haplodiplophasique (présence de deux générations séparées, le gamétophyte haploïde et le sporophyte diploïde) qui devient de plus en plus hétéromorphe, avec prédominance du gamétophyte sur le sporophyte (sporogone)[17].
Généralement, seule une oosphère remplie de réserves et fixée dans son réceptacle est fécondée et conduit à la production d'un sporophyte (monosétie). Il arrive que plusieurs oosphères d'un même réceptacle soient fécondées, aboutissant à la production de plusieurs sporophytes. Ce phénomène est appelé polysétie[18].
Dans certains cas, en particulier chez les anthocérotes, les gamétophytes sont bisexués et nourrissent alors de nombreux sporophytes.
- Après la fécondation, l'embryon matrotrophe est porté par le gamétophyte femelle. Le sporophyte embryonnaire se développe pour donner un sporophyte mature souvent formé d'un pédicelle (plutôt appelé soie chez les mousses et pseudopode chez les sphaignes) portant une capsule. Appelée aussi urne ou sporogone, la capsule correspond au sporange où se forment dans des sporosacs (ou sacs sporifères) les méïospores qui seront à l'origine des gamétophytes. Cette capsule est entourée par une coiffe (appelée aussi calyptre) qui provient du développement de l'archégone. Constituée d'une fine membrane qui protège la capsule, cette coiffe se déchire et disparaît à la maturité du sporophyte. Le sporange libère les spores mâles et femelles (sauf dans le cas des gamétophytes bisexués) qui sont dispersés principalement par le vent (parfois par les mouches chez les Splachnaceae (en)[2]). La plupart des spores tombent au sein de la colonie parentale avant de germiner sous forme de protonema, lequel donne, après une phase de croissance et de développement, les gamétophytes[19].
- Les stades mobiles (en jaune dans le schéma) sont principalement les spores pour lesquelles les mousses ont développé des mécanismes assurant leur dispersion (capsule explosive des sphaignes, fentes de déhiscence des andréales, péristome des vraies mousses) et les anthérozoïdes (ou spermatozoïdes) avant la fécondation.
Les bryophytes peuvent se multiplier de façon végétative par fragmentation (bouturage naturel par brisure de feuilles, de rameaux). Certaines hépatiques ont développé des structures de dispersion spécialisées, les propagules (bourgeon, bulbille). Des structures particulières (gemmules, bulbilles) existent aussi chez certaines mousses[20]. Tous ces éléments sont principalement dispersés par le vent, mais il existe des vecteurs animaux, tels que les chauves-souris[21], les fourmis[22], les limaces[23]. L'allocation des ressources (correspondant à l'allocation de nutriments) reflète l'existence de compromis évolutifs entre deux traits biologiques, la reproduction sexuée favorisée pendant les stades de colonisation et la reproduction asexuée favorisée au sein des colonies matures[24].
Organisation fonctionnelle
Pas de système vasculaire ou un système vasculaire rudimentaire
Les Bryophytes ne disposent pas de xylème ni de phloème (faisceaux conducteurs de l'eau et des nutriments). Ces deux tissus ne sont apparus que plus tard au cours de l'évolution, chez les plantes vasculaires. L'irrigation de l'axe feuillé (appelé caulidie) se réalise par un processus de capillarité, possible grâce à l'étroit agencement des « feuilles » sur cet axe. La « tige » et les « feuilles » (lames foliacées de l'axe) absorbent l'eau et les sels minéraux (puisés dans les eaux de ruissellement qui charrient les éléments minéraux issus de la décomposition des matières organiques et des poussières atmosphériques véhiculées) sur toute leur surface, grâce l'épiderme faiblement cutinisé et constitué de cellules à paroi mince[25]. Cette absorption se fait par imbibition (à travers les surfaces qui peuvent être agrémentées de poils hyalins[Note 4] ou de lamelles parallèles pour augmenter la surface d'échange) puis par diffusion[27].
Certains bryophytes (mousses tropicales, sphaignes) disposent d'ébauches de tissus conducteurs spécialisés permettant le transport de l'eau, des sels minéraux et des produits de la photosynthèse, mais ces derniers ne sont pas lignifiés : les « leptoïdes » (cellules vivantes allongées assurant la distribution des produits de la photosynthèse, l'équivalent de la sève élaborée) et les « hydroïdes » (cellules mortes allongées assurant la distribution de l'eau et des sels minéraux, l'équivalent de la sève brute)[28]. Les mousses endohydriques ont un tissu conducteur développé à la périphérie de l'axe feuillé, les mousses ectohydriques ont seulement des jonctions protoplasmiques entre les cellules, ce qui permet une circulation très localisée des nutriments[29]. Les « feuilles » sont constituées souvent d'une seule assise de cellules chlorophylliennes, excepté dans la région médiane où plusieurs épaisseurs de cellules simulent une nervure différenciée. Le sporophyte présente un épiderme doté de stomates et une ébauche de tissu conducteur au niveau du pédicelle, qui aurait facilité la dessiccation du sporophyte, permettant, à maturité, la déhiscence des capsules et la dispersion des spores[30]. Les stomates, en contrôlant les échanges gazeux (vapeur d'eau, gaz carbonique, oxygène) liés à la photosynthèse et en permettant la régulation des pertes d'eau, sont une innovation évolutive déterminante de la diversification des plantes terrestres. Alors que les ancêtres des plantes terrestres possédaient déjà des stomates, la majorité des mousses auraient perdu ces orifices[31]. Elles auraient subi un processus d'évolution réductive (en) en lien avec leur mode de vie[32].
Les mousses possèdent cependant des tannins complexes proches de la lignine, les lignanes (biopolymères présents dans les vacuoles et les parois cellulaires). Leur appartenance aux métabolites secondaires ainsi que les caractéristiques toxiques, antifongiques ou antibactériennes de certains lignanes font émettre l'hypothèse de leur implication dans les défenses chimiques des plantes contre les herbivores et la photoprotection[33].
Les pseudophylles ou phyllidies n'ont pas l'histologie des vraies feuilles.
Il n'existe pas d'organes comparables aux racines chez les bryophytes dotés de « rhizoïdes » (mono ou pluricellulaires) qui les fixent au substrat mais n'absorbent pas la solution du sol. Les bryophytes ont un cormus (« tige » et « feuille », ces deux organes donnant un axe feuillé). En l'absence de photosynthèse, ce cormus se nécrose, se décolore et forme ainsi un humus primitif.
Les bryophytes ne pouvant absorber l'eau par leur rhizoïdes ont la faculté de permettre à l'eau de rentrer par toutes les parties de la plante. De plus, en cas de forte sécheresse, la plante peut entrer en état de vie ralentie (reviviscence) en attendant des conditions de développement mieux adaptées.
-
Coupe transversale de la « feuille » du Polytric commun[Note 6].
-
Coupe transversale d'une feuille de Philonotis caespitosa montrant la fausse nervure.
Deux grands groupes
Les botanistes du XIXe siècle ont traditionnellement subdivisé les mousses en deux sous-groupes, selon la disposition des sporophytes sur la plante et leur aspect général[36] :
- les mousses acrocarpes (du grec akron, sommet, et carpo, fruit) ont des « tiges » dressées portant à leur extrémité des sporogones. Elles sont très peu ou pas du tout ramifiées, souvent en touffes denses, formant des coussins ou coussinets qui présentent des caractères plutôt xérophiles et héliophiles (en raison de ce port compact en demi-sphère plus apte à lutter contre la forte exposition au soleil et la dessiccation)[Note 7] et une faible longévité ;
- les mousses pleurocarpes (du grec pleuro, côté, et carpo, fruit) ont des « tiges » très ramifiées latéralement d'où émergent les sporogones. Elles sont étalées sur leur support (tiges rampantes), et forment des tapis « moquettes » qui présentent à l'inverse des caractères plutôt hydrophiles et sciaphiles, et une plus grande pérennité du fait des grandes capacités de multiplication végétative des ramifications des tiges[37]. Cette catégorisation pratique souffre de nombreuses exceptions et n'implique pas deux groupes de parenté, même si la monophylie du groupe des pleurocarpes est supportée par des analyses génétiques[38].
-
Développement de mousses en coussins.
-
L'évaporation, en lien avec la taille des coussinets, est un facteur limitant de la photosynthèse[Note 8].
-
Développement de l'Hypne cyprès en tapis étendus plus ou moins denses.
Symbioses avec des champignons
Comme les plantes vascularisées, les bryophytes peuvent profiter d'une symbiose avec des champignons. On a encore peu de connaissances sur la diversité fongique associée aux bryophytes. Mais quelques études basées sur la biologie moléculaire ont montré qu'elle était importante.
Par exemple, en forêt boréale les bryophytes se montrent très résistantes au froid et capables de se nourrir sur des sols gelés tout ou partie de l'année. Les champignons les y aident. Il existe au nord du Canada « un ensemble écologiquement et phylogénétiquement diversifié de champignons associés aux parties vivantes de 3 bryophytes abondantes et largement distribuées (…), les Hylocomium splendens (Hedw.) Schimp. in B.S.G., Pleurozium schreberi (Brid.) Mitt. et Polytrichum commune Hedw »[41]. Au moins 158 espèces de champignons leur sont associées dans la région étudiée. Ces champignons appartiennent surtout à la division des Ascomycota (62,8 % des cas), et à la sous-division des Basidiomycota (32 % des cas), parfois des Chytridiomycota (3,9 % des cas, considérés comme les ancêtres de tous les autres champignons) et rarement aux Glomeromycota (1,3 % seulement des cas, bien que ces champignons soient très fréquemment associés aux plantes supérieures)[41]. Les principaux ordres concernés étaient dans cette région les Helotiales (18,6 %), les Agaricales (11,5 %), les Chaetothyriales (en) (9,6 %) et les Tremellales[41]. L'association la plus souvent repérée était l'agaric Entoloma conferendum avec Lophodermium piceae (Fckl.) Hoehn. comme endophyte associé[41]. D'autres taxons avaient des affinités avec des Helotiales du genre Hyphodiscus (en) ou avec plusieurs basidiomycètes mycorhiziens[41]. La plupart (72,2 %) des taxons de champignons endophytes n'ont été trouvés qu'une seule fois dans cette étude[41]. De plus, très peu de champignons étaient associés avec l'ensemble des trois bryophytes étudiés, ce qui indique une diversité d'associations très large et peut-être certaines spécificités[41], qui restent à explorer.
Autre exemple, Pleurozium schreberi (la Pleurozie dorée) est une mousse qui peut fournir du phosphate et du carbone aux racines du Pin tordu colonisées par le Bolet des bouviers et qui forme des ectomycorhizes avec eux[42].
Habitats et répartition

Capables de tirer leurs nutriments de l'air et des aérosols, comme les lichens qu'ils accompagnent souvent, les bryophytes sont en tant que groupe taxonomique très ubiquistes. Grâce à de nombreuses adaptations, ils ont colonisé presque toute la planète, jusqu'aux zones subpolaires[46]. Ils sont toutefois absents (plus que les lichens) du milieu marin, et des milieux extrêmement arides. Grâce à des spores aéroportées, ils comptent parmi les premières espèces à pouvoir coloniser les nouveaux habitats (ex : terrils, îles volcaniques nouvelles…)
De nombreuses espèces vivent sur le sol (terricoles), dans l'humus (humicoles) ou les milieux tourbeux (turficoles), d'autres sont saxicoles (ou devenues muricoles) ou épiphytes, ou encore se développent sur les bois morts tombés au sol (corticoles sur l'écorce). Dans les réserves naturelles et en forêt dans les îlots de sénescence, après une vingtaine d'années de non-gestion (« restauration passive »[47]), le taux de bois mort au sol ré-augmente au profit des bryophytes notamment[47] mais aussi de nombreux cortèges saproxylophages, chacun caractéristique de l'un des stades de décomposition du bois, et du type d'essence (bois dur, bois tendre, etc.) ou de situation (à l'ombre, au soleil, dans l'eau…)[48].
-
Hypne cyprès, espèce ubiquiste.
-
Riccia fluitans, hépatique flottante utilisée en aquariophilie pour l'oxygénation de l'eau.
-
Eurhynchium praelongum (en)[Note 13], l'Eurhynchie allongée, plante vivace à tige rampante, humo-terricole[49].
-
Mousse des jardiniers, espèce humicole.
-
Rhytidiadelphus squarrosus (en) (l'Hypne squarreux), une des mousses les plus communes des jardins[Note 14].
- Cas de mimétisme avec les mousses
-
Œufs du pluvier doré très mimétiques avec les mousses.
Écologie


Turgescentes, les mousses se gorgent d'eau, un kilogramme de bryophyte sèche pouvant retenir 15 litres d'eau (les capacités d'absorption étant maximisées chez les sphaignes dont un kg peut retenir 70 à 75 litres d'eau)[53].
Les Bryophytes sont généralement autotrophes par photosynthèse grâce aux cellules pourvues de chlorophylle. Certaines en sont dépourvues, telle l'hépatique Cryptothallus mirabilis qui vit sous d'autres mousses en milieu bois. Parasite sur un champignon du genre Tulasnella (lequel forme une ectomycorhize avec des arbres du genre Betula ou Pinus), elle est l'unique hépatique non chlorophyllienne d'Europe et reste associée à des milieux naturels de très grande qualité[54].
Dans une certaine mesure, en empêchant physiquement des graines d'accéder au sol ou en limitant l'accès de la lumière aux graines déjà présentes dans les sols (spectre du rouge notamment, qui déclenche la germination de certaines graines) et/ou par allélopathie, les tapis de mousses peuvent éliminer ou sélectionner certaines espèces[55] ; par exemple dans une pelouse calcaire néerlandaise (et de même en conditions contrôlées en serre), un tapis dense de mousses sur le sol réduit jusqu'à 30 % le nombre de plantules de certaines espèces phanérogames[55].
Les mousses ont un pouvoir absorbant et isolant mis à profit par les rongeurs qui utilisent ce matériau pour tapisser leurs terriers ou par les oiseaux pour leurs nids. Lors de relevés bryophytiques, les bryologues ont distingué 65 espèces de mousses qui garnissaient le nid de passereaux comme les mésanges. Plus de la moitié de la masse de leurs nids est composé de mousses[56].
Malgré le pouvoir nutritif des mousses identique aux plantes vasculaires et le fait qu'elles offrent un habitat à de nombreux invertébrés, elles sont très peu consommées par les herbivores, notamment en raison de la synthèse de composés peu digestes voire inappétents (tanins, terpénoïdes) qui interviennent probablement dans des réactions de défense contre les herbivores[57]. Elles servent de nourriture à quelques espèces de coléoptères, orthoptères, collemboles, chenilles ou pucerons[58] Elles sont plus consommées dans les régions de haute latitude où elles dominent la végétation (zones arctiques et toundras) où elles font partie du régime alimentaire hivernal des ruminants comme le renne et le bœuf musqué[59].
Services écosystémiques

Les mousses fournissent de nombreux services écosystémiques.
Espèces ingénieurs, elles ont la capacité, en s'installant, de créer des micro-habitats qui hébergent une diversité faunistique (un mètre carré de mousses abrite des milliers d'espèces de vers, acariens, rotifères, collemboles, tardigrades, pseudoscorpions, et une entomofaune riche de coléoptères, fourmis) et floristique (lichen, épiphytes telle que les Hyménophyllacées et les orchidées) importantes[61]. Une seule mousse peut abriter des dizaines d'espèces d'invertébrés[62]. Les mousses servent également de site de reproduction à des insectes et acariens[63].
Lorsque les conditions le permettent, les mousses non ramifiées s'installent en colonies formant des tapis et des coussins. À partir des débris issus de la décomposition des micro-organismes hébergés et de la dégradation naturelle des brins à partir de la base de ces colonies, les mousses créent un micro-humus qui favorise leur développement ainsi que celui d'autres espèces végétales[64].
Elles ont pris une place dans le quotidien des humains (serviettes hygiéniques en sphaignes, couches, papier toilette, carburant en Europe, costumes traditionnels en Nouvelle Guinée), en médecine (utilisées en Chine pour leurs vertus médicinales), en agriculture (engrais, phytosanitaire)[65], dans leur foyer (remplissage de matelas ou d'oreiller[Note 15], calfeutrage des habitations en bois, toits végétalisés pour l'isolation, plantes ornementales en aquariophilie) ou dans la construction navale (calfatage des embarcations)[66],[67]. Les chercheurs ont trouvé chez les bryophytes des antibiotiques, des antifongiques, des hormones végétales, des anti-tumoraux[68].
Biosurveillance, environnement et pollution

Les bryophytes, et les mousses en particulier tirent l'essentiel de leur nourriture de l'air et des nutriments apportés par l'eau atmosphérique[70], par la pluie ou les dépôts de particules et aérosols. En raison notamment de leurs grandes capacités d'absorption d'eau et de minéraux passivement, de leur tissu épidermique faiblement cutinisé et constitué le plus souvent d'une seule couche de cellules à paroi mince (ce qui permet d'accroître la capacité d'échange), et de parois cellulaires contenant de nombreux sites de fixation chargés négativement qui capturent les cations métalliques[Note 17], de nombreux bryophytes sont vulnérables à l'acidification de l'air, à sa pollution[72] et à l'eutrophisation des milieux[73].
Ils jouent à ce titre un rôle important dans l'épuration de l'air, mais aussi en matière d'accumulation de certains polluants (métaux lourds et radionucléides notamment). Ce sont aussi des organismes pionniers de succession (capables de croître sur des sols squelettiques et de fournir de l'humus pour les communautés suivantes) importants dans les processus de résilience écologique.
Ils sont moins sensibles à la continuité temporelle de l'état forestier que les lichens[74].
Les espèces les plus sensibles aux polluants acides et aux pesticides véhiculés par l'air ont parfois disparu de tout ou partie de leur habitat naturel. Depuis les années 1960, certaines espèces sensibles ou résistantes sont utilisées comme des bioindicateurs ou des biointégrateurs, en matière de qualité thermohygrométrique de l'air notamment ou de contaminations métalliques (cas des bryophytes aquatiques ou urbaines)[75],[76]. Parmi les bioaccumulateurs végétaux et animaux, les mousses sont ceux qui répondent le mieux aux critères exigibles pour l'obtention d'une bonne information sur le degré de contamination métallique des cours d'eau. Elles permettent notamment de cartographier la pollution présente et d'un passé récent. On les a utilisées par exemple[Note 18] pour cartographier des pollutions par le plomb ou le cadmium[77].
Ils ont aussi été utilisés comme indicateurs de changement climatique récent[78].
Histoire évolutive


Le fossile de mousse Pallavicinites devonicus, daté du dévonien supérieur (environ 350 millions d'années)[80], rappelle que les embryophytes (i.e. les plantes terrestres) sorties des eaux il y a environ 450 millions d'années sont probablement issues d'algues vertes du groupe des charophytes, qui ont évolué en eau douce et sont capables de supporter des émersions temporaires grâce à ces associations symbiotiques (bactéries, micro-algues et micro-champignons)[81].
Les premiers phylums à émerger au sein des bryophytes sont respectivement et successivement les hépatiques à thalle, les anthocérotes et les mousses vraies[82].
La conquête du milieu terrestre exige un certain nombre d'adaptations qui sont toujours présentes chez les mousses actuelles. Faisant partie des premières plantes terrestres pour qui l'eau et le gaz étaient les facteurs limitants, elles avaient certainement peu de possibilités de contrôler leur teneur en eau (absence de stomates au niveau de l'axe feuillé, mince cuticule). Ne possédant ni de vrais vaisseaux conducteurs, ni de véritables racines, ni d'organes de stockage, elles ont développé plusieurs adaptations : grande capacité d'absorption de l'eau (elles fonctionnant pour la plupart comme une éponge), tolérance à la dessiccation et capacité de reviviscence lorsque les conditions extrêmes (sécheresse, climat…) qu'elles ont dû endurer sont terminées[Note 19], ce qui explique que les bryophytes se sont autant affranchies du milieu aquatique que les végétaux vasculaires, beaucoup de mousses survivant dans des milieux secs (par exemple les espèces pionnières capables de coloniser les roches nues, les déserts chauds et froids[Note 20], les toits ensoleillés des maisons)[86]. Elles ont toujours besoin d'eau (par exemple de pluie) pour leur reproduction sexuée aquatique. L'absence de tissus conducteurs pose des problèmes de soutien en raison de la poussée d'Archimède réduite en milieu aérien, d'où leur petite taille qui ne dépasse généralement pas 7 cm et leur forme compacte qui permet à leur appareil végétatif d'acquérir un port dressé qui complète les autres ports typiques (rampant, en coussinet, en lames foliacée)[87],[88]. Elles disposent de rhizoïdes assurant l'ancrage, tandis que l'absorption de l'eau et des minéraux est réalisée par une symbiose fongique avec l'équivalent de mycorhizes[89].
Peu de changements morphologiques sont observés depuis les fossiles jusqu'aux formes actuelles, ce qui fait des bryophytes le groupe le plus stable morphologiquement des plantes terrestres[90].
Les anthocérotes forment un lien important pour l'étude de l'évolution des plantes car il représente un groupe frère des végétaux vasculaires[91]. Ils montrent le passage de la phase gamétophytique dominante au profit du sporophyte dominant des plantes vasculaires (réduction de taille mais aussi du temps de vie du gamétophyte), conduisant au succès évolutif des plantes à fleurs. Une hypothèse est que la réduction de cette phase gamétophytique du cycle biologique au cours de la conquête des terres (milieu difficile) pourrait être que la diploïdie du sporophyte autorise le masquage de l'expression de mutations délétères (provenant d'une exposition aux UV) par complémentation génétique[92],[93].
Taxinomie
Le sous-règne des Bryobiotina a été nommé par le botaniste italien Vittore Benedetto Antonio Trevisan de Saint-Léon en 1876, initialement sous le nom Bryophytae[94].
Liste des divisions (ou phylums) du sous-règne des Bryobiotina (du règne des Chlorobiota) selon J. M. Glime, 2017[5], Novikoff et Barabasz-Krasny, 2015[6] et la World Flora Online (WFO) (5 janvier 2024)[95] :
- Anthocerotophyta Stotl. et Crand.-Stotl. - les anthocérotes
- Bryophyta Schimp. - les mousses
- Marchantiophyta Stotler et Crand. - les hépatiques ou marchantiophytes
Le Catalogue of Life (5 janvier 2024)[96] et bryonames.org[97] ajoutent la division fossile des †Langiophytophyta Doweld, 2001.
Selon Tropicos (13 juin 2023)[98] (attention liste brute contenant des synonymes) :
- Anthocerotophyta Stotler & Crand.-Stotl., 1977
- Bryophyta Schimp., 1879
- Hepaticophyta H.C. Bold ex Stotler & Crand.-Stotl., 1977
- Hepatophyta H.C. Bold ex Stotler & Crand.-Stotl., 1977
- Hepatophyta H.C. Bold, 1957
- † Langiophytophyta Doweld, 2001
- Marchantiophyta Stotler & Crand.-Stotl., 2000
- Monosporangiophyta S. Majumdar, 2020
- Mstikhinia Mosseichik, Ignatov & Ignatiev, 2007
- Sphagnophyta H.A. Crum, 2001
- Takakiophyta Crand.-Stotl., 1986
Avec près de 25 000 espèces de mousses et sphaignes, 9 000 espèces d'Hépatiques (Marchantiophytes) et 300 espèces d'anthocérotes, les bryophytes constituent le second groupe de végétaux terrestres, après les Dicotylédones[99]. En France, près de 1 300 espèces sont connues, le pays comptant de nombreux taxons très rares[100].
La phylogénétique moléculaire actuelle remet en cause les caractères morphologiques utilisés pour la classification classique, en montrant qu'il y a souvent une homoplasie substantielle dans plusieurs de ces caractères employés pour définir des genres, des familles et des sous-ordres[101].
État, pression et menaces sur les populations
Certaines espèces ont disparu de régions entières, ou doivent être considérées comme rares, menacées ou en danger (une liste rouge de bryophytes a par exemple été publiée pour le Luxembourg[102]).
D'autres sont devenues envahissantes.
-
Buxbaumia viridis, espèce protégée en France.
Notes et références
Notes
- Tetraplodon angustatus (sv) est par exemple une espèce coprophage inféodée aux excréments de carnivores (renard, loup et chien) et probablement aussi aux pelotes de réjection de chouettes[1].
- L'étymologie de ce nom scientifique fait référence aux corbeilles en forme de lunule, de croissant, cruciata aux pieds du sporophyte en croix. Ces propagules se forment au fond de la corbeille, puis s'élèvent sur un court pédicule et enfin se détachent.
- Le diagramme représente les « tiges » brunes pour les distinguer des « feuilles » vertes mais ces tiges sont généralement vertes car elles aussi photosynthétiques.
- Ces poils prolongent les « nervures » des « feuilles » et forment des pointes à leur extrémités. Ils réfléchissent la lumière du jour, ce qui permet de lutter contre le dessèchement. Inversement, ils captent les gouttelettes de rosée ou de brouillard grâce à des papilles en surface qui créent des canaux piégeant l'eau. On peut dire ainsi que les mousses vivent d'air et d'eau fraiche[26].
- Cette coupe permet d'observer, de l'extérieur à l'intérieur, une assise superficielle, à valeur d'épiderme ; une zone corticale constituée de cellules parenchymateuse ; un cordon central formé de leptoïdes et d'hydroïdes[34].
- Finement dentée, la feuille ou pseudophylle porte à sa surface supérieure des lamelles chlorophylliennes dressées de 5 à 10 cellules de haut. Le cordon conducteur est normalement composé d'hydroïdes et de leptoïdes. Ces lamelles ont pour effet d'accroître la surface d'échange et de favoriser la diffusion de CO2, facteur limitant chez ces mousses caractérisées par l'absence de stomates au niveau du gamétophyte[35].
- Elles compensent la forte mortalité des gamétophytes (exposition au soleil, dessiccation ou perte d'eau par évapotranspiration) par une production constante, régulière de sporophytes
- Les grands coussinets qui ont un rapport surface/volume plus bas ont une évapotranspiration plus faible, ce qui leur permet de rester hydratés plus longtemps et donc de photosynthétiser pendant quelques heures de plus[39]. Chez Grimmia pulvinata, « en juillet, des coussins hydratés artificiellement et exposés en plein soleil, se dessèchent en quatre heures pour les plus petits contre neuf heures pour les plus gros[40] ».
- La probabilité de dispersion à courte distance est élevée tandis que celle à longue distance est faible.
- La dispersion des spores est directement influencée par l'incidence des facteurs extrinsèques (facteurs topographiques, position par rapport aux autres plantes, facteurs météorologiques tels que vitesse et direction du vent, ensoleillement, turbulence de l'air, humidité et précipitations) et des facteurs intrinsèques (hauteur de libération des spores, saison de reproduction, taille (moyenne entre 10 et 15 μm) et aérodynamisme des spores, vitesse d'éjection…). Certaines mousses expulsent leurs spores à 30 m/s jusqu'à une dizaine de centimètres de hauteur.
- Une étude en Belgique montre que cette moyenne occulte de grandes disparités : 35 % des espèces bryophytes — incluant notamment des espèces rares — sont susceptibles de se déplacer à une vitesse d'environ 25 km en 50 ans[43].
- Ainsi, la production annuelle d'1 m2 de mousse peut aller de 100 millions à 10 milliards de spores[44].
- Du grec rugchos, « bec d'oiseau », et eu, « bien » ; du latin praelongus, « très long », allusion au rostre très long de l'opercule au sommet de la capsule portée par le sporophyte.
- Du grec rhutis, « plis », et diadelphos, « jumelés » (en référence aux deux plis des feuilles caulinaires, bien visibles à sec). Espèce nitrophile et synanthrope, elle n'élimine pas ou n'étouffe pas les herbes du jardin. Comme toutes les mousses des pelouses, elle est moins compétitive que les herbes, disparaît dès leur arrivée et s'installe là où les conditions ne sont pas propices à ces dernières[50].
- D'où l'étymologie populaire associée à l'Hypne cyprès.
- Les feuilles se regroupent en rosettes qui portent des pédicelles dont la couleur varie de vert pâle à jaune orangé, selon leur degré de maturité. Les jeunes capsules portent des coiffes munies d'un long bec.
- Leurs parois ont une teneur élevée en acides polygalacturoniques et groupes fonctionnels (amine, phosphodiester) qui forment des sites immobiles extracellulaires chargés négativement, favorisant les réactions d'échange cationique (remplacement d'un cation lié à ces sites par un autre cation métallique du milieu extérieur). Différentes voies sont généralement décrites pour expliquer la prise en charge des contaminants (métaux, radionucléides) et leur bioaccumulation (adsorption sur la surface des parois cellulaires, transport dans les espaces intercellulaires…)[71].
- Orthotrichum diaphanum (de) est une mousse épiphyte qui vit sur les murs et les trottoirs humides des villes et qui résiste à la pollution urbaine.
- Les bryophytes ont développé la capacité de supporter une période de sécheresse en cessant toute activité métabolique, vie ralentie qui peut atteindre plusieurs siècles comme pour Chorisodontium aciphyllum (en)[83]. Pour résister à la dessiccation, elles fonctionnent comme une éponge et certaines développent certaines adaptations en prenant une apparence brune et rabougrie : crispation des feuilles (de), entortillement, application des feuilles contre la tige, retournement du thalle. Cette phase d'anhydrobiose peut perdurer jusqu'à une trentaine d'années pour certaines espèces[84].
- Cette colonisation de milieux oligotrophes pauvres en azote est permise grâce à l'association symbiotique avec des cyanobactéries du type Nostoc réalisant la photosynthèse et fixant l'azote[85].
Références
- (en) Howard Crum, Structural diversity of bryophytes, University of Michigan Herbarium, , p. 214.
- (en) A. Smith, Bryophyte Ecology, Springer Science & Business Media, , p. 314.
- Jean-Claude Rameau, Dominique Mansion et Gérard Dumé, Flore forestière française : guide écologique illustré, Forêt privée française, , p. 173.
- (en) Tomas Hallingbäck et Nick Hodgetts, Mosses, liverworts, and hornworts: status survey and conservation action plan for bryophytes, IUCN in collaboration with the Swedish Threatened Species Unit, (ISBN 978-2-8317-0466-1).
- (en) Janice M. Glime, « Anthocerotophyta Chapt. 2-8 », dans Bryophyte Ecology, vol. 1, Université technologique du Michigan et International Association of Bryologists (en), (lire en ligne).
- (uk) A. Novikoff et B. Barabasz-Krasny, « Система ембріофітів », dans Modern Plant Systematics [« Système d'embryophytes »], Lviv, Ukraine, Liga-Pres, (lire en ligne [PDF]), p. 23-63.
- Jean-Louis De Sloover et Anne-Marie Bogaert-Damin, Les Muscinées du XVIe au XIXe siècle dans les collections de la Bibliothèque universitaire Moretus Plantin, Presses universitaires de Namur, , p. 103.
- Jean Vallade, L'œil de lynx des microscopistes. La sexualité végétale : l'apport des micrographes depuis le XVIIe siècle, Éditions universitaires de Dijon, , p. 111.
- Johannes Hedwig, Theoria generationis et fructificationis plantarum cryptogamarum Linnæi, Pétersbourg, 1784 [lire en ligne], p. 52 et suiv.
- (en) Anupama Krishna, Botany for Degree Students. Bryophyta, S. Chand Publishing, , p. 12.
- (en) A. Jonathan Shaw et Bernard Goffinet, Bryophyte Biology, Cambridge University Press, (lire en ligne [PDF]), p. 135.
- Karen S. Renzaglia, Juan C. Villarreal et R. Joel Duff, « New insights into morphology, anatomy, and systematics of hornworts », dans Bryophyte Biology, Cambridge University Press, (ISBN 978-0-521-69322-6, DOI 10.1017/cbo9780511754807.004, lire en ligne), p. 139–172.
- Daniel Richard, Martine Hausberger, Patrick Chevalet, Sylvie Fournel, Nathalie Giraud, Frédéric Gros, Patrick Laurenti, Fabienne Pradere, Thierry Soubaya et Frédéric Ysnel, Biologie, Dunod, , p. 115.
- (en) R. E. Longton, « Reproductive biology and evolutionary potential in bryophytes », Journal of the Hattori Botanical Laboratory, vol. 41, , p. 205-223 (lire en ligne [PDF]).
- (en) Kishan Gopal Ramawat, Jean-Michel Mérillon et K. R. Shivanna, Reproductive Biology of Plants, CRC Press, , p. 64.
- (en) Roy C. Brown et Betty E. Lemmon, « Spores before sporophytes: hypothesizing the origin of sporogenesis at the algal–plant transition », New Phytologist, vol. 190, no 4, , p. 875–881 (ISSN 0028-646X et 1469-8137, DOI 10.1111/j.1469-8137.2011.03709.x, lire en ligne, consulté le ).
- Yves Tourte, Michel Bordonneau, Max Henry et Catherine Tourte, Le monde des végétaux. Organisation, physiologie et génomique, Dunod, , p. 48.
- Amélie Pichonet, « Variabilité et dispersion au sein du genre Dicranum Hedw. (Dicranaceae, Bryophyta) : approches moléculaire et morphologique », Thèse Museum National d'Histoire Naturelle, 2011, p. 6.
- Amélie Pichonet, op. cit., p. 7.
- Angela E. Newton et Brent D. Mishler, « The Evolutionary Significance of Asexual Reproduction in Mosses », The Journal of the Hattori Botanical Laboratory, vol. 76, , p. 127–145 (DOI 10.18968/jhbl.76.0_127, lire en ligne [PDF], consulté le ).
- J. G. Parsons, A. Cairns, C. N. Johnson et S. K. A. Robson, « Bryophyte Dispersal by Flying Foxes: A Novel Discovery », Oecologia, vol. 152, no 1, , p. 112–114 (ISSN 0029-8549, lire en ligne [PDF], consulté le ).
- (en) Jörgen Rudolphi, « Ant-mediated dispersal of asexual moss propagules », The Bryologist, vol. 112, no 1, , p. 73–79 (ISSN 0007-2745 et 1938-4378, DOI 10.1639/0007-2745-112.1.73).
- Robin Wall Kimmerer et Craig C. Young, « The Role of Slugs in Dispersal of the Asexual Propagules of Dicranum flagellare », The Bryologist, vol. 98, no 1, 21/1995, p. 149 (DOI 10.2307/3243652).
- (en) Christopher G. Eckert, « The loss of sex in clonal plants », Evolutionary Ecology, vol. 15, no 4, , p. 501–520 (ISSN 1573-8477, DOI 10.1023/A:1016005519651, lire en ligne [PDF], consulté le ).
- (en) J. W. Bates, « Mineral nutrient acquisition and retention by bryophytes », Journal of Bryology, vol. 17, no 2, , p. 223-240 (DOI 10.1179/jbr.1992.17.2.223).
- (en) William McLagan Malcolm, Nancy Malcolm, Mosses and other bryophytes : an illustrated glossary, Micro-Optics Press, , p. 156.
- Franck Massé, Les mousses, les lichens et les fougères, CNPF, , p. 24.
- Vincent Chassany, Marie Potage et Maud Ricou, Biologie végétale, Dunod, , p. 81.
- (en) David H. S. Richardson, The biology of mosses, John Wiley & Sons Canada, , p. 25-26.
- (en) Jeffrey G. Duckett et Silvia Pressel, « The evolution of the stomatal apparatus: intercellular spaces and sporophyte water relations in bryophytes—two ignored dimensions », Philosophical Transactions of the Royal Society B: Biological Sciences, vol. 373, no 1739, , p. 20160498 (ISSN 0962-8436 et 1471-2970, PMID 29254963, PMCID PMC5745334, DOI 10.1098/rstb.2016.0498, lire en ligne, consulté le ).
- « Cladogramme des plantes terrestres, montrant l'évolution des stomates », dans (en) Brogan J. Harris, C. Jill Harrison, Alistair M. Hetherington et Tom A. Williams, « Phylogenomic Evidence for the Monophyly of Bryophytes and the Reductive Evolution of Stomata », Current Biology, vol. 30, no 11, , p. 2001–2012.e2 (ISSN 0960-9822, DOI 10.1016/j.cub.2020.03.048, lire en ligne, consulté le ).
- (en) Bernard Goffinet, Victoria Catherine Hollowell et Robert E. Magill, Molecular Systematics of Bryophytes, Missouri Botanical Garden Press, (lire en ligne), p. 55.
- Marc-André Selosse, Les Goûts et les couleurs du monde. Une histoire naturelle des tannins, de l'écologie à la santé, Actes Sud Nature, , p. 91.
- Valérie Boutin, Jean-François Fogelgesang, Jean-François Beaux et Françoise Ribola, Atlas de biologie végétale, Dunod, , p. 17.
- (en) Mariann Marschall et Michael C. F. Proctor, « Are Bryophytes Shade Plants? Photosynthetic Light Responses and Proportions of Chlorophyll a, Chlorophyll b and Total Carotenoids », Annals of Botany, vol. 94, no 4, , p. 593–603 (ISSN 1095-8290 et 0305-7364, PMID 15319230, PMCID PMC4242232, DOI 10.1093/aob/mch178, lire en ligne, consulté le ).
- (en) Matt von Konrat, Bryophytes. The Closest Living Relatives of Early Land Plants, Magnolia Press, , p. 176.
- Gérard Guillot, « Pierre qui mousse n’amasse pas d’eau », sur zoom-nature.fr, .
- (en) Matt von Konrat, Bryophytes. The Closest Living Relatives of Early Land Plants, Magnolia Press, , p. 180.
- (en) Gerhard Zotz, Anja Schweikert, Walter Jetz et Herta Westerman, « Water relations and carbon gain are closely related to cushion size in the moss Grimmia pulvinata », New Phytologist, vol. 148, no 1, , p. 59–67 (ISSN 0028-646X et 1469-8137, DOI 10.1046/j.1469-8137.2000.00745.x, lire en ligne, consulté le ).
- Gérard Guillot, « La grimmie : une souris grise sur un mur », sur zoom-nature.fr (consulté le ).
- (en) Håvard Kauserud, Cecilie Mathiesen et Mikael Ohlson, « High diversity of fungi associated with living parts of boreal forest bryophytes », Botanique, vol. 86, no 11, , p. 1326-1333 (DOI 10.1139/B08-102, lire en ligne).
- (en) T. J. Carleton & D. J. Read, « Ectomycorrhizas and nutrient transfer in conifer – feather moss ecosystems », Revue canadienne de botanique, vol. 69, no 4, , p. 778-785 (DOI 10.1139/b91-101).
- (en) Virginie Hutsemekers, Claude Dopagne et Alain Vanderpoorten, « How far and how fast do bryophytes travel at the landscape scale? », Diversity and Distributions, vol. 14, no 3, , p. 483–492 (ISSN 1366-9516 et 1472-4642, DOI 10.1111/j.1472-4642.2007.00454.x, lire en ligne, consulté le ).
- (en) C. J. Miles et R. E. Longton, « Deposition of moss spores in relation to distance from parent gametophytes », Journal of Bryology, vol. 17, no 2, , p. 355–368 (ISSN 0373-6687 et 1743-2820, DOI 10.1179/jbr.1992.17.2.355).
- (en) Emma J. Pharo et Charles E. Zartman, « Bryophytes in a changing landscape: The hierarchical effects of habitat fragmentation on ecological and evolutionary processes », Biological Conservation, vol. 135, no 3, , p. 315–325 (DOI 10.1016/j.biocon.2006.10.016, lire en ligne [PDF], consulté le ).
- (en) Royce E. Longton, Biology of Polar Bryophytes and Lichens, Cambridge University Press, coll. « Studies in Polar Research », (ISBN 978-0-521-09338-5, DOI 10.1017/cbo9780511565212, lire en ligne).
- (en) P. Meyer et M. Schmidt, « Accumulation of dead wood in abandoned beech (Fagus sylvatica L.) forests in northwestern Germany », Forest Ecology and Management, vol. 261, no 3, , p. 342–352 (ISSN 0378-1127, DOI 10.1016/j.foreco.2010.08.037).
- Jacques Bardat, « Écologie des Bryophytes », Bulletin Mycologique et Botanique Dauphine-Savoie Spécial bryophytes, vol. 46, no 182, , p. 47–61.
- Jean-Claude Rameau, Dominique Mansion et Gérard Dumé, Flore forestière française. Plaines et collines, Forêt privée française, , p. 89.
- (en) Andrew Farmer et Jeffrey Batesl, Bryophytes and Lichens in a Changing Environment, Clarendon Press, , p. 262
- (en) Scott Hotaling, Timothy C. Bartholomaus et Sophie L. Gilbert, « Rolling stones gather moss: movement and longevity of moss balls on an Alaskan glacier », Polar Biology, vol. 43, no 6, , p. 735–744 (ISSN 0722-4060 et 1432-2056, DOI 10.1007/s00300-020-02675-6, lire en ligne [PDF], consulté le ).
- Franck Massé, Les mousses, les lichens et les fougères, CNPF, , p. 21.
- (en) David H. S. Richardson, The biology of mosses, John Wiley & Sons Canada, , p. 37.
- (en) Martin I Bidartondo, Thomas D Bruns, Michael Weiss, Cecília Sérgio & and David J Read, « Specialized cheating of the ectomycorrhizal symbiosis by an epiparasitic liverwort », Proc Biol Sci., vol. 270, no 1517, , p. 835–842 (DOI 10.1098/rspb.2002.2299).
- B.V. Tooren, « Effects of a bryophyte layer on the emergence of seedlings of chalk grassland species », Acta Oecologica, vol. 11, no 2, , p. 155-163 (lire en ligne)
- (en) Jennifer Britt, Charles Deeming, « First-egg date and air temperature affect nest construction in Blue Tits Cyanistes caeruleus, but not in Great Tits Parus major », Bird Study, vol. 58, no 1, , p. 78-89 (DOI 10.1080/00063657.2010.524916).
- (en) O. O. Oyesiku & O. R. Ogunkolade, « The relationship between the Nigerian garden snail Limicolaria aurora and the moss Hyophila crenulata », Journal of Bryology, vol. 28, no 2, (DOI 10.1179/174328206X105380).
- (en) U. Gerson, « Moss-arthropod association », The Bryologist, vol. 72, , p. 495-500.
- (en) Claudia Ihl & Perry S. Barboza, « Nutritional Value of Moss for Arctic Ruminants: A Test with Muskoxen », The Journal of Wildlife Management, vol. 71, no 3, , p. 752-758.
- (en) Longton, R. E. (1992) The role of bryophytes and lichens in terrestrial ecosystems. In, J. W. Bates & A. M. Farmer (eds). Bryophytes in a Changing Environment, 32-76. Clarendon Press, Oxford
- (en) Alain Vanderpoorten et Bernard Goffinet, Introduction to Bryophytes, Cambridge University Press, , p. 35.
- (en) Bojana Božanić et al, « Factors Affecting Invertebrate Assemblages in Bryophytes of the Litovelské Luhy National Nature Reserve, Czech Republic », Acat Zoologica Bulgarica, vol. 65, no 2, , p. 197-206.
- (en) Gerson U. 1982. Bryophytes and Invertebrates. – In: Smith A. J. E. (Ed.): Bryophyte Ecology. London, New York (Chapman & Hall Ltd), p. 291-332.
- Franck Massé, Les mousses, les lichens et les fougères, CNPF, , p. 25.
- (en) Jan-Peter Frahm, « Recent Developments of Commercial Products from Bryophytes », The Bryologist, vol. 107, no 3, , p. 277-283.
- Sébastien Leblond & Anabelle Boucher, « Initiation à la bryologie - Voyage au cœur de la vie secrète des mousses », 2011, p.24
- C. Ah-Peng, P. Staménoff, J. Bardat, T. Hedderson, L. Marline, N. Wilding, D. Strasberg, « Initiation à l'étude des bryophytes des îles du Sud Ouest de l’océan Indien », 2014, Faculté des sciences Université de la Réunion, p. 6
- (en) Ando, H. & A. Matsuo (1984). Applied bryology, In W. Schultze-Motel (ed.), Advances in Bryology, vol 2 Cramer, p. 133- 224.
- (en) Bernard Clément, Jean Touffet, « Plant strategies and secondary succession on Brittany heathlands after severe fire », Journal of Vegetation Science, vol. 1, no 2, , p. 195-202 (DOI 10.2307/3235658).
- (en) A.M. Kooijman et C. Bakker, « Species replacement in the bryophyte layer in mires: the role of water type, nutrient supply and interspecific interactions », Journal of Ecology, vol. 83, , p. 1–8 (résumé)
- (en) Anju Malik, Mohd. Kashif Kidwai, Vinod Kumar Garg, Bioremediation of Toxic Metal(loid)s, CRC Press, , p. 65
- (en) A.M. Kooijman et C. Bakker, « The acidification capacity of wetland bryophytes as influenced by clean and polluted rain », Aquatic Botany, vol. 48, , p. 133–144 (DOI 10.1016/0304-3770(94)90080-9, résumé)
- (en) A.M. Kooijman (1993), Changes in the bryophyte layer of rich fens as controlled by acidification and eutrophication. PhD Thesis, Utrecht University, the Netherlands
- (en) Ö. Fritz, L. Gustafsson et K. Larsson, « Does forest continuity matter in conservation? - A study of epiphytic lichens and bryophytes in beech forests of Southern Sweden », Biological Conservation, vol. 141, , p. 655–668 (résumé)
- (en) P. C. Onianwa, « Monitoring atmospheric metal pollution: A review of the use of mosses as indicators », Environmental Monitoring and Assessment, vol. 71, no 1, , p. 13–50 (DOI 10.1023/A:1011660727479).
- (en) Maurizio Aceto, Ornella Abollino, Raffaele Conca, Mery Malandrino, « The Use of Mosses as Environmental Metal Pollution Indicators », Chemosphere, vol. 50, no 3, , p. 333-342 (DOI 10.1016/S0045-6535(02)00533-7).
- (en) Theresa Greenaway, Mosses and Liverworts, Steck-Vaughn, , p. 20.
- J.P. Frahm et D. Klaus, « Bryophytes as indicators of recent climate fluctuations in Central Europe », Lindbergia, vol. 26, no 2, , p. 97–104
- R. Wattenhofer, Contribution à l'étude des macrophytes du Léman, Conservatoire Botanique de Genève, , p. 115.
- (en) F. M. Hueber, « Hepaticites devonicus, a New Fossil Liverwort from the Devonian of New York », Annals of the Missouri Botanical Garden, vol. 48, no 2, , p. 125–131 (DOI 10.2307/2394879).
- (en) Douglas E. Soltis, Pamela Soltis, J.J. Doyle, Molecular Systematics of Plants II : DNA Sequencing, Springer, , p. 530
- « Du Silurien au Dévonien : les sorties des eaux », sur cnrs.fr (consulté le ).
- (en) Esme Roads, Royce E. Longton, Peter Convey, « Millennial timescale regeneration in a moss from Antarctica », Current biology, vol. 24, no 6, , p. 222-223 (DOI 10.1016/j.cub.2014.01.053)
- Laurent Burgisser & Ariane Cailliau, « Les mousses » : Liste Rouge, inventaire et initiation aux bryophytes du canton de Genève, Conservatoire et jardin botaniques de la ville de Genève, 2012 , p. 32
- (en) Adams, D. G. & Duggan. P. S. (2008) Cyanobacteria-bryophyte symbioses. Conference Information: Annual Meeting of the Society-for-Experimental-Biology, MAR 31-APR 04, 2007 Glasgow, Scotland. Journal of Experimental Botany 59: 1947-1058
- (en) P. Alpert & M. J. Oliver (2002) Drying without dyin, In: Black M, Prichard HW (eds) Desiccation and survival in plants: drying without dying, CABI, Wallingford, p. 3–43
- (en) Hugues Renault, Annette Alber, Nelly A. Horst, Alexandra Basilio Lopes, Eric A. Fich, Lucie Kriegshauser, Gertrud Wiedemann, Pascaline Ullmann, Laurence Herrgott, Mathieu Erhardt, Emmanuelle Pineau, Jürgen Ehlting, Martine Schmitt, Jocelyn K. C. Rose, Ralf Reski & Danièle Werck-Reichhart, « A phenol-enriched cuticle is ancestral to lignin evolution in land plants », Nature Communications, vol. 8, no 14713, (DOI 10.1038/ncomms14713).
- Peter H Raven, Susan R Singer, Georges B Johnson, Kenneth A Mason, Jonathan B Losos, Biologie, De Boeck Superieur, (lire en ligne), p. 591.
- Jean Garbaye, La symbiose mycorhizienne, Quae, , p. 121.
- (en) R. Reski, « Development, Genetics and Molecular Biology of Mosses », Plant biology, vol. 111, no 1, , p. 10 (DOI 10.1111/j.1438-8677.1998.tb00670.).
- Peter H Raven, op. cit., p. 593
- (en) H. Bernstein, G.S. Byers et R.E. Michod, « Evolution of sexual reproduction: Importance of DNA repair, complementation, and variation », The American Naturalist, vol. 117, no 4, , p. 537–549 (DOI 10.1086/283734).
- (en) R.E. Michod et T.W. Gayley, « Masking of mutations and the evolution of sex », The American Naturalist, vol. 139, no 4, , p. 706–734 (DOI 10.1086/285354).
- (it) Trevisan de Saint-Léon, « Carestiaea, nuovo genere di Andreäacee », Atti Della Società Italiana Di Scienze Naturali, vol. 19, , p. 468–480
- WFO : World Flora Online. Published on the Internet : http://www.worldfloraonline.org., consulté le 5 janvier 2024
- Catalogue of Life Checklist, consulté le 5 janvier 2024
- (en) « The Bryophyte Nomenclator — Bryobiotina », sur www.bryonames.org (consulté le )
- Tropicos.org. Missouri Botanical Garden., consulté le 13 juin 2023
- (en) Buck, W.R. & Goffinet, B. 2000. 3. Morphology and classification of mosses. In A.J. Shaw & B. Goffinet (eds.), Bryophyte Biology. Cambridge University Press, p. 71
- Vincent Hugonnot, Un haut-lieu pour la conservation des bryophytes : les gorges de la Rhue (Cantal), Journée Forêt & Biodiversité du 17 octobre 2013
- (en) B. Crandall-Stotler, R. E. Stotler & D. G. Long, « Morphology and classification of the marchantiophyta », in Goffinet, B., & Shaw, A.J. (eds), Bryophyte Biology, Cambridge University Press, 2008, p. 1–54.
- Werner J (1987) Liste rouge des bryophytes du Grand-Duché de Luxembourg. Musée d'histoire naturelle (PDF, 46 p).
Voir aussi
Bibliographie
- (en) Frey, W., Frahm, J.P., Fischer, E., & Lobin, W. (2006), The Liverworts, Mosses and Ferns of Europe. Harley Books, Colchester
- (en) Goffinet, B., Buck, W.R., & Shaw, A.J. (2008), Morphology, anatomy and classification of the Bryophyta. Pages 55–138 of: B., Goffinet, & A.J., Shaw (eds), Bryophyte Biology second edition. Cambridge University Press.
- Prune Pellet - Bryoflore des pierriers gréseux du massif du Suquet (Aigoual, Cévennes), Répartition, inventaire, caractérisation bryocénotiques et écologiques et évaluation de l'intérêt patrimonial, Rapport de stage Parc National des Cévennes, MNHN. Mis en ligne par Tela-Botanica.
- Vincent Hugonnot, Mousses et hépatiques de Païolive (Ardèche et Gard, France), Jarnac, Société Botanique du Centre-Ouest, , 293 p. (ISSN 0759-934X)
- Vincent Hugonnot, Jaoua Celle, Florine Pépin, Mousses et hépatiques de France, Biotope Editions, 2015, 320 p. (ISBN 9782366621952)
- (en) Alain Vanderpoorten et Bernard Goffinet, Introduction to Bryophytes, Cambridge University Press, , 293 p. (lire en ligne)
Articles connexes
Liens externes
- base de données taxinomique spécialisée sur les bryophytes : (en) « The Bryophyte Nomenclator — Home », sur www.bryonames.org (consulté le )
- (en) Référence BioLib : Bryobiotina D.H. Campbell (consulté le )
- (en) Référence Catalogue of Life : Bryobiotina Trevis. (consulté le )
- (fr + en) Référence EOL : Bryobiotina Trevis. (consulté le )
- (en) Référence Paleobiology Database : Bryobiotina (consulté le )
- (en) Référence Taxonomicon : Bryobiotina Campb. (1890) (consulté le )
- (en) Référence Tropicos : Bryobiotina Trevis. (+ liste sous-taxons) (consulté le )
- (en) Référence World Flora Online (WFO) : Bryobiotina Trevis. (+descriptions) (consulté le )
- Bryophytes, article en ligne de l'Encyclopædia Universalis
- Les bryophytes, présentation du Centre de ressources pédagogiques en Biologie Végétale de l'Université de Bourgogne
- Bryophytes de France
- (en) Bryophyta. Tree of life
- Bryologia Gallica
- Clés de détermination (chapitre 3)

















![Microphotographie d'une coupe transversale de l'axe feuillé de Dawsonia[Note 5].](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d2/Dawsonia_stem.svg/324px-Dawsonia_stem.svg.png)
![Coupe transversale de la « feuille » du Polytric commun[Note 6].](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/Polytrichum_commune_querschnitt.jpeg/240px-Polytrichum_commune_querschnitt.jpeg)


![L'évaporation, en lien avec la taille des coussinets, est un facteur limitant de la photosynthèse[Note 8].](https://upload.wikimedia.org/wikipedia/commons/thumb/2/2c/Polsterkissenmoos_2.jpg/240px-Polsterkissenmoos_2.jpg)




![Eurhynchium praelongum (en)[Note 13], l'Eurhynchie allongée, plante vivace à tige rampante, humo-terricole[49].](https://upload.wikimedia.org/wikipedia/commons/thumb/5/5d/Moss_cobroft_rest_area.jpg/240px-Moss_cobroft_rest_area.jpg)

![Rhytidiadelphus squarrosus (en) (l'Hypne squarreux), une des mousses les plus communes des jardins[Note 14].](https://upload.wikimedia.org/wikipedia/commons/thumb/f/f3/Rhytidiadelphus_squarrosus_141600299.jpg/240px-Rhytidiadelphus_squarrosus_141600299.jpg)
![Mousses de glacier (en) dont les boules peuvent se déplacer de 2,5 cm par jour[51].](https://upload.wikimedia.org/wikipedia/commons/thumb/e/e8/Mousses_sur_le_fell_field%2C_Ditrichum_strictumLycopodium_magellanicum_-_panoramio.jpg/240px-Mousses_sur_le_fell_field%2C_Ditrichum_strictumLycopodium_magellanicum_-_panoramio.jpg)





