The US FDA’s proposed rule on laboratory-developed tests: Impacts on clinical laboratory testing
Contidos

Chámase oxidorredución[1] ou reacción de oxidación-redución ou de redución-oxidación ou reacción redox a toda reacción química na cal os átomos cambien o seu estado de oxidación; en xeral, as reaccións redox implican a transferencia de electróns entre especies químicas.
A reacción pode ser ou ben un proceso redox simple, como a oxidación do carbono para dar dióxido de carbono (CO2) ou a redución do carbono polo hidróxeno para orixinar metano (CH4), ou ben un proceso complexo como a oxidación da glicosa (C6H12O6) no metabolismo humano por medio dunha serie de complexos procesos de transferencia de electróns.
O termo "oxidorredución" ou "redox" procede dos dous conceptos implicados na transferencia de electróns: redución e oxidación,[2] que se poden explicar de maneira simple así:
- Oxidación é a perda de electróns ou un incremento no estado de oxidación dunha molécula, átomo, ou ión.
- Redución é a ganancia de electróns ou unha diminucuión no estado de oxidación dunha molécula, átomo, ou ión.
Aínda que as reaccións de oxidación están xeralmente asociadas coa formación de óxidos ao reaccionar con moléculas de oxíxeno, estes son só exemplos específicos dun concepto máis xeral de reaccións que implican xeralmente a transferencia de electróns.
As reaccións redox teñen varias semellanzas coa reaccións ácido-base. Igual que as reaccións ácido-base, as reaccións redox prodúcense á vez, é dicir, non pode haber unha reacción de oxidación sen que simultaneamente se produza unha reacción de redución. A oxidación por separado e a redución por separado denomínanse cada unha semirreacción, porque as dúas semirreaccións ocorren sempre xuntas para constiruíren a reacción completa redox. Cando se escriben semirreaccións, xeralmente inclúense a ganancia ou perda de electróns explicitamente para que queden equilibradas con respecto á carga eléctrica.
Aínda que estas descricións adoitan ser suficientes para moitos propósitos, non son totalmente precisas. A oxidación e redución realmente refírense a un cambio no estado de oxidación, e pode non haber transferencia real de electróns. Así, a oxidación defínese mellor como un incremento no estado de oxidación, e a redución como unha diminución no estado de oxidación. Na práctica, a transferencia de electróns sempre causa un cambio no estado de oxidación, pero hai moitas reaccións que se clasifican como "redox" e nas que non hai transferencia de electróns (como as que implican a enlaces covalentes).
Os termos oxidante/redutor e oxidado/reducido ás veces orixinan confusión, polo que debe terse en conta o seguinte:
- Oxidante ou axente oxidante é (na definición xeral utilizada) o que capta electróns, polo que o seu estado de oxidación diminúe (polo que el se reduce). Pero ao quitarlle electróns a outra substancia, esa outra substancia oxídase (perde electróns).
- Redutor ou axente redutor é o que cede electróns, polo que o seu estado de oxidación aumenta (polo que el se oxida). Pero ao ceder electróns a outra substancia, esa outra substancia redúcese (gaña electróns).
Etimoloxía
"Redox" é unha abreviación formada por "redución" e "oxidación".
A palabra oxidación orixinalmente implicaba unha reacción co oxíxeno para formar un óxido, xa que o dioxíxeno (O2 (g)) foi historicamente o primeiro axente oxidante recoñecido. Máis tarde, o significado do termo ampliouse para abranguer as substancias similares ao oxíxeno que realizaban reaccións químicas similares. Finalmente, o significado xeneralizaouse incluíndo todos os procesos que implicaban perda de electróns.
A palabra redución orixinalmente referíase á perda de peso que se producía despois de quentar un mineal metálico como un óxido metálico para extraer o metal. Noutras palabras, o mineral era "reducido" a metal. Antoine Lavoisier (1743-1794) demostrou que esa perda de peso debíase á perda de oxíxeno en forma de gas. Posteriormente, descubriuse que o átomo metálico gañaba electróns nese proceso. O significado de redución despois foi xeneralizado para incluír todos os procesos que implicaban ganancia de electróns. Malia que "redución" pode parecer antiintuitivo cando se fala dunha ganancia de electróns, axuda a pensar na redución como unha perda de oxíxeno, que era un dos seus significados históricos.
O electroquímico John Bockris utilizou as palabras electronación e deselectronación para describir os procesos de redución e oxidación, respectivamente, cando ocorren en eléctrodos.[3] Estas palabras son análogas a protonación e desprotonación, pero non foron adoptadas apenas polos químicos.
O termo "hidroxenación" podería utilizarse no lugar de redución, xa que o hidróxeno é o axente redutor nun gran número de reaccións, especialmente en química orgánica e bioquímica. Pero, a diferenza de oxidación, que foi xeneralizada a partir do seu elemento raíz, hidroxenación mantivo a súa conexión específica coas reaccións que engaden hidróxeno a outra substancia (por exemplo, a hidroxenación de graxas insaturadas a graxas saturadas, R-CH=CH-R + H2 → R-CH2-CH2-R).
Axentes oxidantes e redutores
Nos procesos redox, o redutor transfire electróns ao oxidante. Así, na reacción, o redutor ou axente redutor perde electróns e é oxidado, e o oxidante ou axente oxidante gaña electróns e é reducido. O par formado por un axente oxidante e un axente redutor implicados nunha determinada reacción denomínase par redox. Un par redox é unha especie química reducida xunto coa súa forma oxidada, por exemplo, Fe2+/Fe3+.
Oxidantes
As substancias que teñen a capacidade de oxidar a outras substancias (facendo que perdan electróns) dise que son oxidantes ou oxidativas e denomínanse axentes oxidantes ou oxidantes. É dicir, o oxidante (axente oxidante) quita electróns doutra substancia, e dese modo el queda reducido. Como "acepta" electróns, o axente oxidante tamén se chama aceptor de electróns. O oxidante prototípico é o oxíxeno.
Os oxidantes son xeralmente substancias químicas que teñen elementos con altos estados de oxidación (por exemplo, peróxido de hidróxeno (H2O2), permanganato (MnO4-), trióxido de cromo (CrO3), dicromato (Cr2O72-), óxido de osmio (VIII) (OsO4), ou substancias cos elementos máis electronegativos (oxíxeno (O2), flúor (F2), cloro (Cl2), bromo (Br2]]), todos os cales poden gañar facilmente electróns extra oxidando outras substancias.
Redutores
As substancias que teñen a capacidade de reducir outras substancias (o que fai que esas substancias gañen electróns) dise que son redutoras ou redutivas e denomínanse axentes redutores ou redutores. O redutor (axente edutor) transfire electróns a outras substancias, e así el queda oxidado. Como "doa" electróns, o axente redutor denomínase tamén doante de electróns. Os doantes de electróns poden tamén formar complexos de transferencia de carga con aceptores de electróns.
Os redutores en química son moi diversos. Os metais elementais electropositivos, como o litio, sodio, magnesio, ferro, cinc, e aluminio, son bos axentes redutores. Estes metais doan ou ceden electróns doadamente. Os reactivos de transferencia de hidruros, como o NaBH4 e o LiAlH4, son amplamente usados en química orgánica,[4][5] principalmente na redución de compostos de carbonilo a alcohois. Outro método de redución implica o uso de gas hidróxeno (H2) cun catalizador de paladio, platino, ou níquel. Estas reducións catalíticas utilízanse principalmente na redución de enlaces carbono-carbono dobres ou triplos.
Potenciais de redución
Cada semirreacción ten un potencial estándar de eléctrodo (E0cell), que é igual á diferenza de potencial (ou voltaxe) (E0cell) no equilibrio nas condicións estándar dunha cela electroquímica na cal a reacción do cátodo é a semirreacción considerada, e o ánodo é un eléctodo de hidróxeno estándar no que se oxida o hidróxeno: ½ H2 → H+ + e-.
O potencial de eléctrodo de cada semirreacción tamén se denomina potencial de redución E0red, ou potencial medido cando a semirreacción ten lugar nun cátodo. O potencial de redución é unha medida da tendencia de que o axente oxidante sexa reducido. O seu valor é cero para H+ + e− → ½ H2 por definición, positivo para axentes oxidantes máis fortes que o H+ (por exemplo, +2.866 V para o F2) e negativo para axentes oxidantes que son máis febles que o H+ (por exemplo, –0.763 V para o Zn2+).[6]
Para unha reacción redox que teña lugar nunha cela, a diferenza de potencial é E0cela = E0cátodo – E0ánodo
Porén, o potencial da reacción no ánodo era ás veces expresado como potencial de oxidación, E0ox = – E0. O potencial de oxidación é unha medida da tendencia do axente redutor a ser oxidado, pero non representa o potencial físico nun eléctrodo. Con esta notación, a ecuación de voltaxe na cela escríbese cun signo máis (+) E0cell = E0cátodo + E0ox (ánodo)
Exemplos de reaccións redox

Un bo exemplo é a reacción entre o hidróxeno e o flúor, na cal o hidróxeno é oxidado e o flúor é reducido:
- H2 + F2 → 2 HF
Esta reacción global pódese escribir como dúas semirreaccións:
A semirreacción de oxidación é:
- H2 → 2 H+ + 2 e−
e a semirreacción de redución é:
- F1 + 2 e− → 2 F−
Analizar cada semirreacción por separado xeralmente fai máis claro o proceso químico global. Como non hai carga neta durante unha reacción redox, o número de electróns en exceso na reacción de oxidación debe igualar o número consumido pola reacción de redución (como se mostra arriba).
Os elementos, mesmo cando están én forma molecular, sempre teñen un estado de oxidación de cero. Na primeira semirreacción, o hidróxeno oxídase desde un estado de oxidación de cero a un estado de oxidación de +1. Na segunda semirreacción, o flúor redúcese desde un estado de oxidación de cero a un estado de −1.
Cando se suman as dúas semirreaccións os electróns cancélanse:
H2 → 2 H+ + 2 e− F2 + 2 e− → 2 F−
H2 + F2 → 2 H+ + 2 F−
E os ións combínanse para formar fluoruro de hidróxeno:
- 2 H+ + 2 F− → 2 HF
A reacción global é:
- H2 + F2 → 2 HF
Desprazamento de metais

Neste tipo de reacción, un átomo metálico dun composto (ou en solución) é substituído por un átomo doutro metal. Por exemplo, o cobre deposítase cando o metal cinc se sitúa nunha solución de sulfato de cobre(II):
Zn(s)+ CuSO4(aq) → ZnSO4(aq) + Cu(s)
Na reacción anterior, o metal cinc despraza ao ión cobre(II) da solución de sulfato de cobre e así libera metal cobre libre.
A ecuación iónica para esta reacción é:
- Zn + Cu2+ → Zn2+ + Cu
Escribindo as dúas semirreaccións, vese que o cinc se oxida:
- Zn → Zn2+ + 2 e−
E o cobre redúcese:
- Cu2+ + 2 e− → Cu
Outros exemplos
- A redución do nitrato a nitróxeno en presenza de ácido (desnitrificación):
- 2 NO3− + 10 e− + 12 H+ → N2 + 6 H2O
- A combustión de hidrocarburos, como nun motor de combustión interna, que produce auga, dióxido de carbono, algunhas formas parcialmente oxidadas como o monóxido de carbono, e enerxía calorífica. A oxidación completa de materiais que conteñan carbono produce dióxido de carbono.
- En química orgánica, a oxidación paso a paso dun hidrocarburo polo oxíxeno produce auga e, sucesivamente, un alcohol, un aldehido ou unha cetona, un ácido carboxílico, e despois un peróxido.
Corrosión e enferruxamento


- O termo corrosión refírese á oxidación electroquímica de metais nunha reacción cun oxidante como o oxíxeno. O enferruxamento ou oxidación do ferro, que é a formación de óxidos de ferro, é un bo exemplo de corrosión electroquímica; orixínase como resultado da oxidación do metal ferro. A ferruxe común xeralmente é óxido de ferro(III), formado na seguinte reacción química:
- 4Fe + 3O2 → 2Fe2O3
- A oxidación do ferro(II) a ferro(III) polo peróxido de hidróxeno en presenza dun ácido é:
- Fe2+ → Fe3+ + e−
- H2O2 + 2 e− → 2 OH−
- A ecuación global é:
- 2 Fe2+ + H2O2 + 2 H+ → 2 Fe3+ + 2 H2O
Reaccións redox na industria
A protección catódica é unha técnica usada no control da corrosión da superficie dun metal facendo que este sexa o cátodo dunha cela electroquímica. Un simple método de protección conecta o metal protexido a un "ánodo sacrificial" máis fácil de corroer, que actúa como ánodo. O metal sacrificial é o que se corroe en lugar do metal protexido. Unha aplicación da protección catódica é o aceiro galvanizado, no cal unha cuberta sacrificial de cinc sobre o aceiro protexe a este da oxidación.
O proceso primario de reducir minerais a alta temperatura para producir metais coñécese como fundición.
A oxidación utilízase en moitas industrias como na produción de produtos de limpeza e de amoníaco oxidante para producir ácido nítrico, o cal se usa na maioría dos fertilizantes.
As reaccións redox son o fundamento das celas electroquímicas.
O proceso de galvanoplastia utiliza reaccións redox para cubrir obxectos cunha fina capa dun material, como nas pezas de automóbiles cromadas, xogo de cubertos prateados, e xoiaría cuberta con capas de ouro e prata.
A produción de discos compactos depende dunha reacción redox, que cobre o disco cunha fina capa de película metálica.
Reaccións redox en bioloxía

|
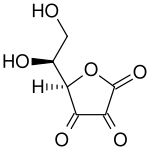
|
Abaixo: ácido deshidroascórbico (forma oxidada da vitamina C)
As reaccións redox están implicadas en moitos procesos biolóxicos importantes.
A respiración celular, por exemplo, é a oxidación de compostos orgánicos como a glicosa (C6H12O6) a CO2 e a redución de oxíxeno a auga. Faise por medio de numerosos pasos intermedios nos que se van orixinando compostos orgánicos cada vez máis oxidados. A ecuación global da respiración é:
- C6H12O6 + 6 O2 → 6 CO2 + 6 H2O
O proceso da respiración celular depende de forma fundamental da redución do coencima NAD+ a NADH e da reacción inversa (a oxidación do NADH ao NAD+). Os coencimas recollen os electróns procedentes dos substrantos que se están oxidando, e despois poden volvelos a ceder. Na respiración actúa unha cadea de transporte de electróns na cal os transportadores sofren sucesivas oxidacións-reducións, de modo que un transportador da cadea é o aceptor de electróns do membro anterior da cadea, e o doante de electróns do membro seguinte da cadea. Os coencimas levan electróns á cadea procedentes dos substratos "respirados" (oxidados) e lévanos ata o aceptor final, que é o oxíxeno na respiración aerobia (ou outra substancia na respiración anaerobia). Durante a circulación de electróns créase un gradiente de protóns, o cal impulsa a síntese de ATP.
A fotosíntese tamén comprende reaccións redox, e na fase luminosa actúa unha cadea de transportadores de electróns e fórmase NADPH, que se utiliza para reducir o CO2. Globalmente os electróns circulan desde o H2O (doante de electróns) ao NADPH e despois ao CO2:
- 6 CO2 + 6 H2O + luz → C6H12O6 + 6 O2
As reaccións de radicais libres son reaccións redox do sistema defensivo do organismo, que ocorren como parte do mantemento da homeostase, e serven para matar microorganismos. Nelas despréndese un electrón dunha molécula e despois vólvese a captar case instantaneamente. Os radicais libres son un tipo de moléculas redox e poden ser nocivas para o corpo humano se non rexeneran a molécula redox ou se unen a un antioxidante. Os radicais libres poden favorecer as mutacións nas células e os cancros.
O termo estado de oxidación utilízase a miúdo para describir o balance do GSH/GSSG, NAD+/NADH e NADP+/NADPH nun sistema biolóxico como unha célula ou órgano. O estado redox reflicte o equilibrio de varios conxuntos de metabolitos (por exemplo, lactato e piruvato, beta-hidroxibutirato, e acetoacetato), cuxa interconversión depende das súas proporcións. Un estado redox anormal pode orixinar varias situacións daniñas, como hipoxia, shock circulatorio, ou sepse. Os mecanismos redox tamén controlan varios procesos celulares. As proteínas redox e os seus xenes deben estar colocalizados para a regulación redox segundo a hipótese CoRR do funcionamento do ADN nas mitocondrias e cloroplastos.
Ciclos redox
Unha gran variedade de compostos aromáticos son reducidos encimaticamente para formar radicais libres que conteñen un ou varios electróns máis que os seus compostos parentais. En xeral, o doante de electróns é algún flavoencima e os seus coencimas. Unha vez formados, estes radicais libres aniónicos reducen moléculas de oxíxeno a superóxido, e rexeneran o composto parental. A reacción neta é a oxidación dos coencimas do flavoencima e a redución do oxíxeno molecular para formar superóxido. Este comportamento catalítico foi descrito como un ciclo fútil ou ciclo redox.
Exemplos de moléculas que inducen ciclos redox son os herbicidas paraquat e outros violóxenos e quinonas como a menadiona.[7]
Reaccións redox en xeoloxía

En xeoloxía, as reaccións redox son importantes tanto para a formación de minerais coma para a mobilización de minerais, e tamén nalgúns medios sedimentarios.
Axuste de reaccións redox
Para describir a reacción electroquímica global dun proceso redox hai que equilibrar ou axustar os compoñentes das semirreaccións para a oxidación e a redución. En xeral, para reaccións en solución acuosa, isto implica engadir H+, OH−, H2O, e electróns (e−) para compensar os cambios na oxidación.
Medio ácido
En medio ácido, engádense ións H+ e auga ás semirreaccións para axustar a reacción global.
Por exemplo, cando o manganeso(II) reacciona co bismutato de sodio:
Reacción sen axustar: Mn2+(aq) + NaBiO3(s) → Bi3+(aq) + MnO4−(aq) Oxidación: 4 H2O(l) + Mn2+(aq) → MnO4−(aq) + 8 H+(aq) + 5 e− Redución: 2 e− + 6 H+ + BiO3−(s) → Bi3+(aq) + 3 H2O(l)
A reacción está equilibrada axustando as dúas reaccións de semicela para que interveñan o mesmo número de electróns (multiplicando a reacción de oxidación polo número de electróns no paso da redución e viceversa):
- 8 H2O(l) + 2 Mn2+(aq) → 2 MnO4−(aq) + 16 H+(aq) + 10 e−
- 10 e− + 30 H+ + 5 BiO3−(s) → 5 Bi3+(aq) + 15 H2O(l)
Sumando estas dúas reaccións elimínanse os electróns e obtense a reacción axustada:
- 14 H+(aq) + 2 Mn2+(aq) + 5 NaBiO3(s) → 7 H2O(l) + 2 MnO4−(aq) + 5 Bi3+(aq) + 5 Na+(aq)
Medio básico
En medio básico, engádense ións OH− e auga ás semirreaccións para axustar a reacción global.
Por exemplo, na reacción entre o permanganato potásico e o sulfito sódico:
Reacción sen axustar: KMnO4 + Na2SO3 + H2O → MnO2 + Na2SO4 + KOH Redución: 3 e− + 2 H2O + MnO4− → MnO2 + 4 OH− Oxidación: 2 OH− + SO32− → SO42− + H2O + 2 e−
Axustando o número de electróns nas dúas reaccións de semicela obtense:
- 6 e− + 4 H2O + 2 MnO4− → 2 MnO2 + 8 OH−
- 6 OH− + 3 SO32− → 3 SO42− + 3 H2O + 6 e−
Sumando estas dúas reaccións de semicela obtemos a ecuación axustada:
- 2 KMnO4 + 3 Na2SO3 + H2O → 2 MnO2 + 3 Na2SO4 + 2 KOH
Notas
- ↑ Definicións no Dicionario da Real Academia Galega e no Portal das Palabras para oxidorredución. Consultado o 8 de febreiro de 2017.
- ↑ "Redox Reactions". wiley.com.
- ↑ John O'M. Bockris and Amulya K. N. Reddy (1970). Modern Electrochemistry. Plenum Press. pp. 352–3.
- ↑ Hudlický, Miloš (1996). Reductions in Organic Chemistry. Washington, D.C.: American Chemical Society. pp. 429. ISBN 0-8412-3344-6.
- ↑ Hudlický, Miloš (1990). Oxidations in Organic Chemistry. Washington, D.C.: American Chemical Society. pp. 456. ISBN 0-8412-1780-7.
- ↑ Valores de potencial de eléctrodo tomados de: R.H.Petrucci, W.S.Harwood and F.G.Herring (2002). General Chemistry (8th ed.). Prentice-Hall. p. 832.
- ↑ "gutier.doc" (PDF). Consultado o 2008-06-30. 2,76 MiB
Bibliografía
- Schüring, J., Schulz, H. D., Fischer, W. R., Böttcher, J., Duijnisveld, W. H. (editors)(1999). Redox: Fundamentals, Processes and Applications, Springer-Verlag, Heidelberg, 246 pp. ISBN 978-3-540-66528-1 (pdf 3,6 MB)
- Tratnyek, Paul G.; Grundl, Timothy J.; Haderlein, Stefan B., eds. (2011). Aquatic Redox Chemistry. ACS Symposium Series 1071. ISBN 9780841226524. doi:10.1021/bk-2011-1071.
Véxase tamén
Outros artigos
- Electroquímica
- Equivalente electrónico
- Cadea de transporte electrónico
- Hidroxenación
- Adición oxidativa
- Oxidación parcial
- Pro-oxidante
- Potencial de redución
Ligazóns externas
- Axuste de ecuacións químicas - Un axustador de ecuacións químicas de fonte libre que traballa con reaccións redox.
- Vídeo - Síntese do acetato de cobre(II)- 31 de xullo de 2014
- Calculadora de reaccións redox
- Reaccións redox en Chemguide
- Equilibrador de reaccións redox online, equilibra reaccións de semicelas e reaccións completas



















