The US FDA’s proposed rule on laboratory-developed tests: Impacts on clinical laboratory testing



En botanique, la racine est l'organe souterrain d'une plante servant à la fixer au sol et à y puiser l'eau et les éléments nutritifs nécessaires à son développement. Prolongement de la tige vers le bas (pas toujours, la racine peut être issue de la radicule, organe embryonnaire, lorsque la tige est issue de la tigelle), elle en diffère par plusieurs caractères : sa structure interne, son géotropisme positif, la présence d'une coiffe terminale et de poils absorbants, l'absence de feuilles et de bourgeons. C'est ce dernier caractère qui la distingue fondamentalement de la tige.
Les racines sont souvent le siège de symbioses avec les bactéries et les champignons du sol, en particulier pour le métabolisme de l'azote. Les racines peuvent présenter des adaptations afin de faciliter le développement de la plante dans un environnement particulier (exemple des racines du palétuvier). Dans certains cas les racines servent aussi à stocker des nutriments (exemple du radis, la betterave, le navet, etc.). Certaines racines de plantes sont comestibles ou à usage médicinal, d'autres sont hautement toxiques.
Les racines sont les organes cibles des herbicides racinaires, qu'on emploie pour lutter contre les adventices.
Rôles de la racine

La racine est un organe vital de la plante, qui se forme très tôt lors du développement de la plante, dès le début de la germination. Elle a plusieurs rôles au sein de la plante :
- ancrage au sol (sol plus ou moins meuble) ou sur une paroi ; selon la granulométrie du substrat, les racines ligneuses, dont le diamètre peut aller de quelques millimètres à plusieurs décimètres, se développent et se ramifient plus ou moins. l'aspect du système racinaire change généralement d'une espèce de plante à une autre : un chêne a des racines développées en profondeur, alors qu'un peuplier a un système racinaire de surface[3]. « Une défaillance de cet ancrage peut causer des chablis ou un pivotement irréversible de l’arbre qui peut avoir des conséquences à long terme sur la forme de la tige et la qualité du bois produit. D’un autre côté, un ancrage trop rigide ne peut absorber suffisamment d’énergie et peut ainsi engendrer la casse du tronc (volis)[4] » ;
- fonction de tuteur. Certains végétaux développent des racines aériennes (situées au-dessus de la surface du sol) qui ont pour origine des méristèmes apicaux racinaires situés dans une partie plus haute de la plante qu'habituellement. Ces racines ont une fonction de tuteur en s'ancrant dans le sol de part et d'autre de la plante et en l'empêchant de se courber ;
- absorption de l'eau et des nutriments du sol, et leur transport au reste de la plante pour sa croissance et aux feuilles pour la photosynthèse. Le transport est réalisé par l'évaporation foliaire tractante principalement (évapotranspiration), mais aussi par la pression racinaire due à l'absorption active d'eau (visible lors de la guttation au niveau des hydatodes foliaires) ;
- l'accumulation de réserves. Cette fonction a un rôle primordial dans les régions à climat saisonnier contrasté : pendant la saison défavorable, une partie de ces réserves est utilisée pour la respiration d'entretien des divers tissus ; pendant la saison favorable, le redémarrage de la croissance est facilité par la mobilisation de ces ressources qui sont essentiellement sous forme de glucides (sucres solubles et amidon stockés dans le parenchyme ligneux de l'aubier des branches et des racines), de lipides (surtout des triglycérides, comme dans le cas des Ailanthus sp.) et de protéines de réserve (albumines, globulines, prolamines stockées dans le phloème)[5] ;
- support d'associations symbiotiques complexes avec les micro-organismes (bactéries et champignons) qui vont, par exemple, aider à la solubilisation du phosphore, à la fixation de l'azote atmosphérique, au développement de racines secondaires ;
- décolmatage du sol ;
- création de sol. Les molécules et enzymes sécrétés par les racines et leurs manchons symbiotiques contribuent à la formation du sol. Les racines de nombreux arbres sécrètent des acides organiques assez puissants pour ronger les pierres calcaires et en libérer le calcium et d'autres minéraux utiles pour les espèces qui produisent et exploitent l'humus ;
- communication. Certaines espèces d'arbres peuvent anastomoser leurs racines à celles d'arbres de la même espèce et ainsi mettre en commun des ressources hydriques et nutritives. Ces anastomoses peuvent aider une souche ou un arbre gravement blessé à survivre et à mieux résister à l'érosion des sols, pentes et berges[6]. Quand la connexion n'est pas directement physique, des communications via le tissu mycorhizien peuvent exister. L'anastomose ne doit pas être confondue avec la production d'un nouvel arbre (clone) à partir d'une racine.
On a découvert que des linéaires d'arbres, des bosquets, voire des parties importantes de forêts pouvaient être anastomosés, ce qui laisse supposer qu'il s'agit d'un avantage évolutif important, alors que l'anastomose est suspectée de pouvoir aussi — a priori — être l'occasion du passage rapide de pathogènes d'un arbre à l'autre lorsque l'un des arbres est infecté.
-
De nombreux arbres tropicaux ont des racines et contreforts solides leur permettant de pousser sur des milieux a priori hostiles, Angkor Vat, Cambodge.
-
Dans toutes les forêts primaires les racines exploitent volontiers les nutriments du bois mort, ici au fur et à mesure de sa décomposition, qui facilite la mycorhization des radicelles, réserve de parc national Pacific Rim, Colombie-Britannique, Canada.
-
Les racines jouent un rôle majeur dans le maintien des berges, Schwielowsee, Brandebourg, Allemagne.
Structure de la racine
Morphologie
La jeune racine présente, en partant de son extrémité, une zone embryonnaire qui constitue le pôle de croissance, protégée par une coiffe conique composée de cellules subérifiées se renouvelant constamment. Cette coiffe, par la sécrétion de polyosides, a un rôle lubrifiant afin de permettre une meilleure pénétration de la racine dans le sol. Au sein de la coiffe, des cellules spécifiques, les statocytes, sont impliquées dans la perception de la gravité grâce à leurs statolithe. Suit une zone d'allongement limitée à quelques millimètres, suivie par une zone pilifère (ou assise pilifère). Dans cette dernière zone, chaque poil absorbant (ou trichoblaste, ou poil racinaire) est constitué d'une seule cellule très allongée à grande vacuole, dont les parois nues permettent l'absorption de l'eau et des sels minéraux par osmose. La présence de ces nombreux poils permet d'augmenter considérablement la surface d'absorption de la racine. Ces poils meurent très vite et sont remplacés par d'autres au fur et à mesure de la croissance de la racine, ce qui fait que la zone pilifère est globalement toujours de la même taille. La zone suivante est une couche de cellules enrichies en subérine appelée assise subéreuse. Les racines secondaires issues du péricycle situé autour du faisceau conducteur, permettent d'accroître l'étendue du tissu racinaire. Leur morphologie est comparable à celle de la racine principale. Les plus fines racines secondaires sont appelées les radicelles et comportent généralement beaucoup de poils absorbants.
Les racines fines représentent moins de 10 % de la masse totale d'un arbre mais forment un chevelu racinaire (appelé aussi tapis racinaire) qui correspond à 90 % de sa longueur. Les arbres dans les sols riches peuvent développer plusieurs millions d'extrémités de ces racines fines par mètre carré et sur 30 cm de profondeur[7].
Chez les plantes ligneuses coexistent deux types de racines (phénomène connu sous le nom d'hétérorhizie, caractéristique des arbres à ectomycorhizes) : les macrorhizes (littéralement « racines longues ») qui sont des racines secondaires de structure, assurant l’ancrage mécanique et explorant le sol sur de grandes distances ; les brachyrhizes (littéralement « racines courtes »), racines primaires analogues à des feuilles souterraines, l'activité photosynthétique en moins[8]. Ces racines fines absorbent l’eau et les sels minéraux du sol et sont le siège de la symbiose ectomycorhizienne[9]. Comme les feuilles, elles disparaissent en automne et se reconstituent au printemps. Cette perte racinaire est estimée au tiers de la biomasse racinaire totale, formant une « litière souterraine »[10].
Types de racines spécialisées


- racines pivot ; chez certaines plantes, une partie des racines s'enfoncent verticalement, assurant la stabilité de la plante.
- racines adventives : ce sont des racines qui apparaissent le long d'une tige, spécialement dans les entre-nœuds ;
- racines-crampons : sorte de racines adventives qui permettent à la plante de s'accrocher à son support (lierre) ;
- racines aériennes : développées par les plantes épiphytes pour absorber l'humidité atmosphérique ;
- racines internes : ce sont des racines adventives qui peuvent se développer à l'intérieur du tronc creux d'un arbre vivant, qui vont prélever l'humus produit là par des organismes saproxylophages (si cet humus est assez humide). L'arbre peut alors paradoxalement croître vers son centre et restaurer une écorce interne. À ne pas confondre avec certains champignons (armilaires) qui peuvent tapisser les cavités du bois et qui ont une forme dite rhizomorphe, c'est-à-dire rappelant celle des racines.
- racines tubérisées (en tubercule) : adaptation à l'accumulation de réserves, généralement d'amidon ou d'inuline, dans les différents tissus des racines (exemple de la ficaire, du dahlia, de la betterave sucrière) ;
- racines succulentes : adaptées au stockage de l'eau ;
- racines-échasses : ce sont des racines adventives, plus ou moins arquées, ancrées dans le sol. Cette structure est typique de certains palétuviers poussant dans les mangroves (ex. : Rhizophora spp.). Cette structure a généralement une fonction stabilisatrice pour des espèces poussant sur des sols meubles (ex. : Pandanus spp.) ou d'étai pour le tronc ou les branches (ex. : figuier banian). Les racines-échasses peuvent parfois être garnies d'épines comme chez les palmiers Socratea exorrhiza ou Eugeissona utilis, entre autres.
- racines contreforts : ce sont des empattements racinaires remontant le long du tronc et stabilisant les arbres. Cette structure est souvent présente chez les espèces poussant sur des sols meubles (ex. : Pterocarpus officinalis, fromager...).
- pneumatophores : racines verticales qui émergent de l'eau et permettent d'assurer les échanges gazeux chez certains arbres des marécages et de la mangrove (exemple : cyprès chauve, Taxodium distichum);
- racines suçoirs : observées chez les plantes parasites comme le gui (Viscum album, Loranthacées).
-
Racines échasses du palétuvier.
-
D'autres espèces tropicales poussent sur des échasses, ici garnies d'épines, hors de zones inondées, pour des raisons évolutives non élucidées (Guyane).
-
Racines pneumatophores de Taxodium ascendens
-
Racines-contreforts de fromager.
-
Racines échasses sur Eugeissona utilis
Différentes formes de racines
La racine peut avoir différents aspects : grêle (1), filiforme, pivot (2) ; (3) et fasciculée (4) pour les herbes. Elles peuvent aussi former un caudex comme chez le baobab.
(1) |
(2)
|
(3) |
(4)
|
 |
|
 |

|
Ramification




Chez les plantes herbacées ou ligneuses, une fois la racine pivotante principale formée, la ramification met en place des racines secondaires, tertiaires, etc. créées à partir d'un tissu spécialisé de la racine, le péricycle. Ce tissu forme une masse de cellules méristématiques qui se différencient et prolifèrent vers l'extérieur de la racine, pour former une racine latérale. De nouveaux faisceaux conducteurs de sève se forment ensuite dans cette nouvelle racine.
En outre, des racines adventives peuvent apparaître sur les tiges, soit aux nœuds, soit aux entre-nœuds, voire sur les feuilles (ce qui permet de multiplier les bégonias par des boutures de fragments de feuilles). Les tiges souterraines émettent des racines adventives, de même que les tiges rampantes appelées stolons (exemple du fraisier).
Les botanistes distinguent trois types de ramifications racinaires chez l'arbre mature[13] :
- les racines ligneuses principales (racines pivotantes verticales qui constituent le réseau plongeant et charpentières horizontales ou obliques qui constituent le réseau traçant)[14] qui assurent l’ancrage de l’arbre ;
- les racines ligneuses de prospection qui jouent un rôle d’exploration du sol (racines latérales ramifiées secondaires, tertiaires, etc. qui peuvent dans certains cas prendre beaucoup d'importance par rapport au pivot central) et dont le développement est fonction des ressources disponibles ;
- les racines non ligneuses (les radicelles constituant le chevelu racinaire, et les mycorhizes formant le réseau mycorhizien) qui assurent l’absorption de l’eau et des éléments nutritifs ainsi que leur stockage.
La structuration du système racinaire, ou architecture racinaire, s'organise au cours du temps et est l'expression d'un équilibre entre des processus endogènes de croissance (croissance primaire en longueur et secondaire en diamètre des racines, ramification intrinsèque et réitération, processus sous fort contrôle génétique) et des contraintes extérieures exercées par le milieu (sol, climat, etc.). La typologie de l'architecture racinaire chez les arbres fait l'objet de nombreuses études qui classent les systèmes racinaires en fonction de trois critères (pourcentage de racines obliques[15], importance des fourchaisons spontanées[16], avec sans développement retardé[17]). Les botanistes simplifient la classification et en distinguent traditionnellement trois grands types chez les végétaux herbacés et ligneux[18] :
- système racinaire pivotant : développement prédominant de la racine principale, par la dimension de sa « balle » (largeur et profondeur), système fréquent chez les dicotylédones ;
- système racinaire fasciculé (en cœur) : racines adventives disposées en faisceau à la base de la tige (poireau, plantain) ou racines latérales de même « balle » que la racine principale et non ramifiées (Poacées), système fréquent chez les Monocotylédones ;
- système racinaire traçant : racine principale peu développée, racines latérales à extension horizontale et à faible profondeur (peupliers, résineux qui adoptent ce système lors de conditions édaphiques et climatiques difficiles). Soumises à des stress mécaniques importants, les racines traçantes développent une croissance radiale dissymétrique qui tend à leur donner une forme de poutre en « I » ou en « T » qui offre une meilleure résistance aux efforts verticaux[19].
La forme de l'architecture racinaire dépend des propriétés du sol (tassement, pierrosité, humidité, texture du sol) et des stress mécaniques (vent, pente, direction générale d’inclinaison des troncs à la suite d'une tempête)[15].
L'expression « l'arbre cache la forêt » qui s'applique à la partie aérienne (tronc et houppier) de l'arbre concerne aussi son système racinaire (racines principales, racines secondaires et radicelles) qui est invisible, car son importance est toujours sous-estimée. La portion visible ne représente que la partie émergée car le système racinaire chez les arbres se développe en moyenne — ordre de grandeur à relativiser car il existe une grande variabilité — sur 100 m2 et prospecte un volume de 100 m3 (chiffre à multiplier par 10 pour un chêne âgé en sol non contraignant)[20]. Le système racinaire constitue 10 à 20 % de la biomasse totale de l'arbre, 10 à 50 % de la biomasse de la plante cultivée et 50 à 80 % de la végétation herbacée prairiale[21]. Chez les plantes terrestres, ce système représente en moyenne un tiers de la biomasse totale de la plante et reçoit de 25 à 60 % des produits de la photosynthèse[22],[23]. Les champignons mycorhiziens qui existent chez environ 90 % des plantes vasculaires (par provocation, il est tentant avec ce chiffre de dire que « les plantes, dans leur état naturel, ont des mycorhizes plutôt que des racines[24] ») développent un mycélium racinaire représentant jusqu'à 30 % de la biomasse racinaire[25]. Chez un pin taeda de 48 ans d'âge, la répartition de la biomasse est la suivante : tronc 62,4 % ; branches 15,2 % ; feuillage 2,4 % ; racines pivotantes 11 % ; racines latérales 6,8 % ; racines fines 2,2 %[26].
Les études sur le système racinaire des plantes non ligneuses donnent également des résultats insoupçonnés. Ainsi[27], « un pied d'avoine sans concurrence produirait environ 86 kilomètres de racines au cours d'une seule saison, alors qu'un pied normal n'en élabore à peine qu'un kilomètre ». Un seul plant de seigle « produit 14 millions de racines en quatre mois, soit 500 kilomètres, à un rythme qui peut atteindre 5 kilomètres par jour[28] ».
Une idée reçue veut que le système racinaire est limité à l'espace défini par la projection au sol du houppier, les racines couvrant la même surface au sol que le houppier. En réalité, la majorité des racines tapissent le sol plutôt qu'elles ne le pénètrent et certaines racines horizontales s'étendent jusqu'à des longueurs égales à trois fois la hauteur de l'arbre[29]. L'évolution du système racinaire va généralement d'un cône renversé étroit et profond à un cône renversé à la base très large et peu profond. Le rapport du diamètre du houppier au diamètre de la surface explorée par les racines est en moyenne de l'ordre de 1/2, celui des surfaces respectives varie de 1 à 5[30].
Anatomie
La racine peut présenter deux types successifs de structure : la structure primaire (fig. 1) chez les jeunes plantules, et la structure secondaire (fig. 2) chez les plantes plus âgées mais uniquement chez les Dicotylédones et les Gymnospermes.
Structure primaire
 |
 |
Il s'agit de la structure anatomique des jeunes racines. Sur une coupe transversale (dans le sens de la largeur : voir fig. 1 ci-dessus) d'une telle racine, on distingue deux zones :
- l'écorce : distincte de ce que l'on appelle également l'écorce dans le langage courant, cette partie est constituée du rhizoderme qui porte d'abord les poils absorbants de la racine (ou assise pilifère) puis une couche de cellules subérisées (l'assise subéreuse, lorsque la racine vieillit), et du parenchyme cortical, qui assure le transport des éléments absorbés jusqu'au centre de la racine pour leur transport à travers toute la plante. La dernière couche de cellules de ce parenchyme est épaissie et forme une sorte de barrière de contrôle des molécules circulant dans la racine, c'est l'endoderme.
- le cylindre central : c'est ici que se trouvent les tissus de transport de la sève, de la racine vers le reste de la plante. Il est composé tout d'abord du péricycle, une couche de cellules à partir de laquelle vont se former les ramifications de la racine. Viennent ensuite les deux types de tissus conducteurs, le xylème (ou bois) qui conduit la sève brute vers les feuilles et le phloème (ou liber) qui redistribue la sève élaborée dans toute la plante. Ces deux types de tissus, issus d'une couche intermédiaire de procambium, sont disposés en cercle, alternativement. Enfin, au centre de la racine, la moelle, composée de parenchyme médullaire, n'a pas de fonction particulière (si ce n'est un rôle de réserve).
Structure secondaire

Cette structure ne se met en place que chez les plantes pluriannuelles (mais pas chez les Monocotylédones). C'est l'apparition d'un cambium continu, qui apparait d'abord, en coupe, sous une forme étoilée, qui devient progressivement circulaire avec la croissance de la racine en épaisseur. Le cambium vasculaire (ou assise libéro-ligneuse) va créer les tissus de conduction secondaires que sont le xylème II et le phloème II. Le phellogène (situé vers la périphérie de la racine (ou assise subéro-phellodermique), crée quant à lui une couche externe de suber (ou liège) ainsi qu'une couche plus interne de phelloderme, toutes deux assurant la protection de la racine.
Croissance racinaire

La croissance racinaire est une fonction du méristème apical localisé dans la zone d'élongation (cf. Morphologie). Les cellules méristématiques se divisent plus ou moins de façon continue, et produisent d'autres méristèmes, les cellules de la coiffe et des cellules souches indifférenciées. Ces dernières vont devenir les tissus primaires de la racine.
Les racines vont généralement croître dans toute direction présentant les bonnes conditions en air, nutriments, et eau pour satisfaire aux besoins de la plante. Les racines ne pousseront pas dans un sol sec. Avec le temps, si les conditions sont favorables, les racines peuvent casser fondations, conduites d'eau souterraines, et soulever le trottoir. À la germination, les racines croissent vers le bas sous l'effet du gravitropisme (mécanisme de croissance de la plante, opposable à l'héliotropisme de la tige qui la pousse à croître vers la source de lumière). Certaines plantes, disposant de racines-crampons (comme le lierre grimpant) grimpent aux murs et sur les autres végétaux. C'est ce qu'on appelle le thigmotropisme.
La plupart des plantes croissent par leur partie apicale ; c'est la croissance primaire ou principale, qui permet la croissance verticale. D'un autre côté, la croissance secondaire permet la croissance en diamètre des racines. Déjà évoquée dans le chapitre Anatomie (fig. 2), la croissance secondaire se produit à partir du cambium vasculaire et du cambium cortical.
Chez les plantes ligneuses, le cambium vasculaire, qui se forme à partir du procambium entre le xylème et le phloème primaire, forme un cylindre de tissu tout au long de la racine. Cette couche forme de nouvelles cellules vers l'intérieur (qui se différencient en xylème secondaire) et l'extérieur (qui se différencient en phloème secondaire) du cylindre de cambium. Comme ces tissus secondaires de xylème et phloème se développent, le périmètre de la racine augmente. Conséquemment, les tissus au-delà du phloème secondaire (le parenchyme), ont tendance à être poussés et écrasés contre la paroi.
À cet endroit, le cambium cortical, qui se forme à partir du péricycle, commence à créer de nouvelles cellules selon le même schéma : vers l'extérieur va se former le suber (ou liège), et vers l'intérieur le phelloderme.
Rhizogenèse

La formation des racines, appelée rhizogenèse, est conditionnée par plusieurs facteur limitants : disponibilité en sels minéraux, en sucres, température, lumière et développement foliaire (stimulation de la ramification racinaire par la croissance des feuilles et le développement de racines[31].
« Similaire à la chute périodique des feuilles, la mortalité et le renouvellement cyclique des racines fines est un processus naturel qui intervient constamment au cours du développement de l'arbre. Les racines fines ont une longévité le plus souvent inférieure à un an. Elles se renouvellent une ou plusieurs fois pendant plusieurs années à peu près aux mêmes points sur les racines ligneuses. Ce renouvellement est particulièrement coûteux en énergie : plus de 50 % du carbone assimilé par photosynthèse est alloué à la production des racines fines (cas de Picea abies, Lebègue et al[32], 2004)[33]. »
Racine et génie végétal
Le génie végétal utilise les racines pour fixer, dépolluer ou décolmater certains sols ou sédiments.
Inversement, sur des digues étroites ou fragiles (sables, limons fins peu cohérents) l'action du vent sur les arbres ou la putréfaction des racines après la mort des arbres peuvent être des sources de dégradation de la digue[34].
Une meilleure connaissance de l'autécologie d'une essence forestière peut aider le forestier et l'agrosylviculteur ou un pépiniériste à mieux « installer chaque essence à sa place »[35] dont en fonction de ses capacités d'enracinement de chaque essence[36]
Reconnaissance du soi et du non-soi ?
Savoir si les plantes détectent les racines de leurs voisines, y répondent et si oui, comment et à quelles conditions, est crucial pour bien comprendre les biocénoses et améliorer l'agroécologie.
Si ce n'était pas le cas, les plantes ne seraient régulées que par la biodisponibilité des ressources dans l'air, les pluies et leur zone de prospection racinaire. Mais on sait depuis longtemps que certaines plantes réagissent à leurs voisines par l'évitement, ou parfois par des associations synergiques. Par exemple en 2001, Gersani et al. ont montré que le soja produit plus de racines en présence de concurrents de la même espèce[37].
Les racines, au moins chez certaines espèces, détectent les racines des plantes voisines et y répondre différemment selon l'identité de chaque voisine (i.e. si ces racines sont émises par la même plante, par un clone, par un individu physiologiquement différent, d'un génotype différent ou d'une espèce différente[38].
Ceci peut avoir une grande importance dans les milieux pauvres en ressources, hydriques notamment. Dans les années 1990, Mahall & Callaway (1991, 1996), ont prouvé que des individus de plantes buissonneuses de désert Ambrosia dumosa et de Larrea tridenta avaient des capacités de reconnaissances et d'interactions de type racine-racine. Dans ce cas le système racinaire d' Ambrosia dumosa se montre capable de détecter et éviter les racines d'autres Ambrosia dumosa, alors que les racines de Larrea tridenta inhibent la croissance d'autres Larrea tridenta et Ambrosia dumosa autour d'elles[39],[40], ce qu'ont confirmé en 1995 Krannitzi & Caldwell pour Pseudoroegneria spicata, Agropyron desertorum et Artemisia tridentata[41]. Falik et al. en 2003 ont démontré le même type de phénomène chez Pisum sativum alors qu'au même moment Nishiwaki faisait de même chez Miscanthus sinensis Anderss[42].
En 2003, des chercheurs, sur la base de données écophysiologiques, estiment que les racines sont pour la plante un lieu de discrimination du soi et du non-soi, bien qu'elle ne dispose pas de réseau neuronal semblable à celui des animaux[43]. Ces notions de relations entre racines d'un même individu et entre racines de clones de la même d'espèces et d'individus de la même espèce ou d'espèces différentes, notamment vis-à-vis de la concurrence pour les ressources[38], ont des répercussions en écologie végétale et générale[44],[38].
McConnaughay & Bazzaz (1991) et Loh et al. (2003) ont réussi à séparer les effets de la biodisponibilité en termes de volume de sol et de nutriments biodisponibles[45],[46]. Le mécanisme de ces communication est encore mal compris, mais Semchenko et al., en 2007, en utilisant des types de partitionnement racinaire combinés à du charbon actif absorbant ou adsorbant les exsudats racinaires, ont pu partiellement inverser l'inhibition de la croissance racinaire due au partitionnement des pots, sans toutefois modifier les interactions avec les individus voisins[47]. En 2007 De Kroon invite à répéter ces expériences, dont en utilisant plus d'espèces végétales non-légumineuses, pour exclure un éventuel biais lié aux symbiotes racinaires[38].
Défense contre les pathogènes
Les racines des plantes sont capables de produire une réaction immunitaire pour se défendre contre les pathogènes du sol. La réaction immunitaire a besoin de 2 signaux différents pour être déclenchée.
- Le premier est la détection de dommages cellulaires. La présence de structures cellulaires normalement internes dans l’environnement provoque une surexpression des récepteurs de reconnaissance de motifs moléculaires (PRR acronyme pour : pattern-recognition receptor) dans les cellules bordant la zone endommagée de la racine.
- Le deuxième est la détection de motifs moléculaires associés aux microbes (MAMP acronyme pour : microbe-associated molecular pattern). Un MAMP connu est la protéine bactérienne appelée flagelline. Les MAMPs vont se lier aux PRRs surexprimés dans les cellules à proximité des cellules endommagées et induire la réponse immunitaire dans ces cellules[48].
Fonctions

Outre les fonctions de reconnaissance décrites ci-dessus, les botanistes distinguent les fonctions suivantes chez les racines :
- ancrage superficiel au sol et stabilisation du végétal. Chez les arbres ce rôle mécanique a plus pour effet une « augmentation de la cohésion des couches superficielles que d'un véritable ancrage profond… Quant au poids des arbres, considéré souvent à tort comme un facteur aggravant, il faut relativiser son impact en le comparant à l'épaisseur d'une couche de sol de poids équivalent. Bien souvent, le poids des arbres ne représente pas plus de 5 de couche de sol. Mais l'effet de levier dû à la prise au vent élevée peut entraîner des arrachages »[49] ;
- nutrition : absorption d'eau et de sels minéraux. Les chercheurs en biologie végétale ont longtemps considéré que cette fonction était assurée par les poils absorbants. Or ceux-ci ne sont actifs qu'en période de germination[50], avant que 90 % des plantes ne soient colonisées par des hyphes du champignon symbiote, formant des mycorhizes qui sont les véritables structures assurant l'absorption d'eau et des nutriments[51]. Les poils ne sont fonctionnels que dans quelques groupes de plantes (moins de 10 %) non mycorhizés : ce sont essentiellement des plantes de milieux pionniers (absence de champignons) ou riches, dans lesquels l'approvisionnement hydrominéral ne nécessite pas de mycorhize[52]. Deux chercheurs ont mis en évidence en 1989 le phénomène de redistribution hydrique racinaire[53] ;
- mise en réserve (tubérisation, racine pivotante) de protéines et de produits de la photosynthèse qui sont stockés dans les racines ;
- effet rhizosphère, les racines assurant une interface avec des organismes vivants (micro-organismes et faune du sol) ;
- excrétion : les racines excrètent des exsudats organiques et minéraux favorables au développement du microbiote du sol. L'exsudation « représente une dérivation vers le sol de 5 à 20 % du carbone fixé par la photosynthèse, en fonction des facteurs environnementaux (température, lumière, humidité, contraintes physiques, statut nutritionnel, présence de micro-organismes)[54] ».
Profondeur des racines

La distribution des racines des plantes vasculaires dans le sol dépend de la forme des plantes, de la distribution spatiale et temporelle de l'eau et des nutriments, et des propriétés physiques du sol lui-même. Les racines les plus profondes se rencontrent en général dans les déserts et dans les forêts tempérées de conifères ; les moins profondes se trouvent dans la toundra, dans les forêts boréales et dans les prairies tempérées. Dans une roche-mère fissurée, les racines pivots peuvent poursuivre leur extension verticale. Le record d'enracinement en France est de 150 mètres de profondeur pour des chênes, 140 mètres pour des merisiers ou 110 mètres pour des ormes, comme l'ont rapporté des spéléologues[55] explorant des grottes souterraines[56].

Les stratégies d'occupation du milieu souterrain par les systèmes racinaires se résument en deux grandes situations : une exploration extensive du sol qui s'effectue par la périphérie du système ou une exploration et une exploitation intensives du sol dans laquelle tout le système racinaire intervient. En général, la plupart des racines actives des arbres qui assurent l'absorption des ions minéraux et de l'eau sont des racines superficielles (entre 50 et 80 % selon les espèces et les milieux, situées dans les 20 à 30 premiers centimètres du sol) formant le chevelu racinaire caduc à court terme, les racines ligneuses pérennes (racines superficielles et profondes dont le diamètre est supérieur à 1 cm) qui constituent la charpente racinaire assurant essentiellement l'ancrage et les racines ligneuses caduques se spécialisant dans la colonisation et l'exploitation du sol[57].
Records de profondeur
| Espèce | Localisation | Profondeur maximale (m) | Références[58],[59] |
|---|---|---|---|
| Boscia albitrunca | Désert du Kalahari | 68 | Jennings (1974) |
| Juniperus monosperma | Plateau du Colorado | 61 | Cannon (1960) |
| Eucalyptus sp. | Forêt australienne | 61 | Jennings (1971) |
| Acacia erioloba | Désert du Kalahari | 60 | Jennings (1974) |
| Prosopis juliflora | Désert de l'Arizona | 53.3 | Phillips (1963) |
Les racines et l'humain


Importance économique
Dès l'Antiquité existaient des professions de rhizotomos ῥιζοτόμος / rhizotómos, « coupeur de racine » (ramasseur de plantes, herboriste) et de φαρμακοπώλης / pharmakopôlês, « vendeur de drogues, de médicaments ». Le rhizotome se chargeait de la cueillette des plantes qu'il remettait au pharmacopole (médecin-pharmacien) ayant la responsabilité de la composition des remèdes et de la vente[60]. Au Moyen Âge, les végétaux sont relégués au bas de l'échelle de la Scala naturæ. Les légumes souterrains, aliments non nobles selon la conception occidentale, sont des plantes de mortification alimentaire ou de pénitence[61]. La culture de légumes-racines (betterave sucrière, igname) reste encore aujourd'hui d'une importance économique relativement grande.
Les racines étaient utilisées pour fabriquer certaines pièces de charpenterie navale, le bois tors; plutôt que d'être coupés, les arbres étaient déracinés pour prélever les précieuses courbes[62].
Les souches laissées après l'abattage des arbres sont maintenant parfois extraites du sol pour fournir du bois-combustible aux centrales à biomasse.
Interactions avec le patrimoine bâti
Certains systèmes racinaires peuvent interagir avec les infrastructures proches[63],[64] ou s'insinuer dans certains joints de maçonneries (joints humides faits de terres ou de chaux hydraulique naturelle faiblement dosée). De même dans les sols pauvres et drainants et secs en été, les racines peuvent se diriger vers les réseaux d'eaux pluviales[65] et/ou d'eaux usées (égouts) en écartant les joints de tuyaux de béton[66],[67] ou en s'insinuant dans les joints d'étanchéité de tuyaux de PVC[68] pour aller se développer dans les eaux usées riche en matières organiques. Un programme de recherche européen piloté par la Suède ou ce phénomène a été très étudié a montré qu'il est possible de détourner les racines et d'éviter cela[69], notamment en entourant le tuyau d'un feutre-antiracine. Programme européen de travail piloté par la Orjan Stal Sverige[70]. Quand elles manquent d'eau, des racines peuvent pénétrer presque tous les types de joints de tuyaux de béton ou de pvc[71].
Intérêt pour la biomimétique
De nombreuses propriétés racinaires (croissance adaptative et capacités d'échange avec le milieu notamment) intéressent la biomimétique.
Plusieurs projets de hardwares, softwares, senseurs, actionneurs et robots s'inspirant des systèmes racinaires pour produire des systèmes robotiques pouvant explorer un environnement (sédiments, sol, etc.) en y détectant des ressources ou conditions particulières[72], pour éventuellement dans le futur pouvoir exploiter ces ressources, analyser et suivre (monitoring) des sols, les dépolluer, explorer un nouveau milieu, etc.
Illustrations
-
Principaux types de racines (« pivot », « en chevelu »..).
-
Structure fractale de type racine, modélisée informatiquement.
-
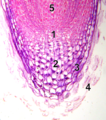
Pointe racinaire (microscope).
-
Présentation pédagogique des racines d'un arbre, vue de dessous.
-
Exemple d'adaptation au substrat.
-
Berge érodée et surpiétinée, mais maintenue par les racines.
-
Racines mises à nu par l'érosion.
-
Racines limitant le phénomène d'érosion.
-
Racines d'arbre tombé et mort ; habitat d'invertébrés spécifique.
-
Système racinaire de sequoia géant.
-
Racines de Pandanus
-
Racines aériennes (Metrosideros excelsa).
-
Racine aérienne d'une liane (Hedera helix).
-
Racines aquatique libre de saule.
-
Contreforts de Ficus variegata, Sulawesi
-
Contreforts du genre Ceiba (Amazonie péruvienne).
Notes et références
- Les anastomoses entre individus de la même espèce permettent aux racines des arbres abattus en éclaircie de survivre et de s'intégrer au système racinaire d'arbres voisins vivants.
- Christophe Drénou, « Uni par les racines », Forêt-Entreprise, vol. 153, , p. 34-38.
- Drénou 2006, p. 25.
- F. Danjon, T. Fourcaud, « L'arbre et son enracinement », Revues Innovations Agronomiques, vol. 6, , p. 17 (lire en ligne).
- Drénou 2006, p. 26.
- (en) Erin C. Fraser, Victor J. Lieffers et Simon M. Landhäusser, The persistence and function of living roots on lodgepole pine snags and stumps grafted to living trees (Résumé
- Drénou 2006, p. 27.
- Francis Hallé, « Des feuilles souterraines ? », Alliage, no 64, , p. 90
- (en) J. Kubikova, « Contribution to the classification of root systems in woody plants », Preslia, vol. 39, , p. 236-243
- Ernst Zürcher, Les arbres, entre visible et invisibl, Actes Sud Nature, (lire en ligne), p. 187.
- ZRT pour « Zone of Rapid Taper » (zone de défilement rapide), partie des racines traçantes proche de la souche. Cf (en) Eis S., 1972. Root system morphology of western hemlock, western red cedar, and douglas-fir. Canadian Journal of Forest Research 4, 28-38.
- Yves Birot, op. cit., p. 169[réf. non conforme]
- Drénou 2006, p. 69-84.
- Ces charpentières sont portées par le collet ou le pivot primaire. Elles développent à leur face inférieure des pivots secondaires.
- (de) J.N. Köstler, E. Brueckner , H. Bibelriether, Die Wurzeln der Waldbäume. Hamburg, Paul Parey, , 284 p..
- Claire Atger, 1992. Essai sur l'architecture des arbres. Thèse de doctorat, Université de Montpellier II, 287 p.
- (en) C. Atger & C. Edelin, « Stem and root tree architecture: Questions for plant biomechanics », Biomimetics, vol. 2, no 3, , p. 253-266.
- (en) M. Busgen, E. Munch, T. Thomas, The structure and life of forest trees, Chapman and Hall, , p. 59.
- Yves Birot, Guy Landmann et Ingrid Bonhême, La forêt face aux tempêtes, éditions Quae, (lire en ligne), p. 176.
- (en) S. Eis, « Root systems of older immature hemlock, cedar, and Douglas-fir », Revue canadienne de recherche forestière, vol. 17, no 11, , p. 1348-1354 (DOI 10.1139/x87-208).
- (en) Hans-Peter Blume, Gerhard W. Brümmer, Heiner Fleige, Rainer Horn, Ellen Kandeler, Ingrid Kögel-Knabner, Ruben Kretzschmar, Karl Stahr, B.-Michael Wilke, Scheffer/Schachtschabel Soil Science, Springer, (lire en ligne), p. 45 et 409
- Marc-André Selosse, Jamais seul. Ces microbes qui construisent les plantes, les animaux et les civilisations, Éditions Actes Sud, (lire en ligne), p. 31
- Marc-André Selosse, L'origine du monde. Une histoire naturelle du sol à l'intention de ceux qui le piétinent, Actes Sud Nature, , p. 456.
- Jean-François Briat et Dominique Job, Les sols et la vie souterraine. Des enjeux majeurs en agroécologie, Editions Quae, , p. 252.
- (en) Jonathan Leake, David Johnson, Damian Donnelly, Gemma Muckle, Lynne Boddy & David Read, « Networks of power and influence: the role of mycorrhizal mycelium in controlling plant communities and agroecosystem functioning », Revue canadienne de botanique, vol. 82, no 8, , p. 1016–1045 (DOI 10.1139/b04-060).
- (en) David H. Van Lear, Jack B.Waide, Michael J. Teuke, 1983. . e 30(2):., « Biomass and nutrient content of a 41-year-old loblolly pine (Pinus taeda L.) plantation on a poor site in South Carolina », Forest Science, vol. 30, no 2, , p. 395-404.
- (en) T. K. Pavlychenko, « Root systems of certain forage crops in relation to the management of agricultural soils », Nat. Res. Council Bull., no 1088, , p. 46.
- Jean-Marie Pelt, La vie sociale des plantes, Fayard, , p. 87.
- Drénou 2006, p. 291.
- (en) B.B. Stout, « ,Studies of the root systems of deciduous trees », Black Rock Forest Bulletin, no 15, , p. 1–45.
- (en) Sophie de Dorlodot, Brian Forster, Loïc Pagès, Adam Price, Roberto Tuberosa, Xavier Draye, « Root system architecture: opportunities and constraints for genetic improvement of crops », Trends in Plant Science, vol. 12, no 10, , p. 474-481 (DOI 10.1016/j.tplants.2007.08.012)
- Lebègue Claire, Laitat Éric, Perrin Dominique, Pissart Geneviève, « Mise en œuvre de carottages de sol et de minirhizotrons pour l'étude à long terme de la réponse des fines racines d'épicéa (Picea abies (L.) Karst.) à l'augmentation de la concentration en CO2 dans l'atmosphère et la nutrition minérale », Biotechnology, Agronomy, Society and Environment, vol. 8, no 1, , p. 41-53
- Drénou 2006, p. 65-66.
- L'enracinement des arbres dans les digues en remblai : étude des systèmes racinaires et impacts sur la sécurité des ouvrages Zanetti, C. ; Vennetier, M. ; Meriaux, P. ; Royet, P. ; Dufour, S. ; Provansal, M. - 2008, Ingénieries no 53 - mars 2008 ; p. 49-67
- Masson G (2005) Autécologie des essences forestières: comment installer chaque essence à sa place. Ed. Tec & Doc
- Lebourgeois F & Jabiol B (2002) Enracinements comparés des chênes (sessile et pédonculé) et du hêtre sur différents matériaux. Réflexions sur l’autécologie des essences. Rev. For. Fr, 54, 17-42.
- (en) Mordechai Gersani, Joel s. Brown, Erin E. O'Brien et Godfrey M. Maina, « Tragedy of the commons as a result of root competition: Game theory and root competition », Journal of Ecology, vol. 89, no 4, , p. 660–669 (DOI 10.1046/j.0022-0477.2001.00609.x, lire en ligne, consulté le )
- (en) Linde Hess et Hans De Kroon, « Effects of rooting volume and nutrient availability as an alternative explanation for root self/non-self discrimination », Journal of Ecology, vol. 95, no 2, , p. 241–251 (DOI 10.1111/j.1365-2745.2006.01204.x, lire en ligne, consulté le )
- (en) B. E. Mahall et R. M. Callaway, « Root Communication Mechanisms and Intracommunity Distributions of Two Mojave Desert Shrubs », Ecology, vol. 73, no 6, , p. 2145–2151 (DOI 10.2307/1941462, lire en ligne, consulté le )
- (en) B. E. Mahall et R. M. Callaway, « Root communication among desert shrubs », Proceedings of the National Academy of Sciences, vol. 88, no 3, , p. 874–876 (ISSN 0027-8424 et 1091-6490, PMID 11607151, PMCID PMC50916, DOI 10.1073/pnas.88.3.874, lire en ligne, consulté le )
- (en) P.G. Krannitzi et M.M. Caldwell, « Root growth responses of three Great Basin perennials to intra and interspecific contact with other roots », Flora, vol. 190, no 2, , p. 161–167 (DOI 10.1016/S0367-2530(17)30647-3, lire en ligne, consulté le )
- données non publiées, dans De Kroon et al.2003, cité en notes et références
- Omer Falik, Perla Reides, Mordechai Gersani et Ariel Novoplansky, « Self/Non-Self Discrimination in Roots », Journal of Ecology, vol. 91, no 4, , p. 525–531 (ISSN 0022-0477, lire en ligne, consulté le )
- (en) M. Gruntman et A. Novoplansky, « From The Cover: Physiologically mediated self/non-self discrimination in roots », Proceedings of the National Academy of Sciences, vol. 101, no 11, , p. 3863–3867 (ISSN 0027-8424 et 1091-6490, PMID 15004281, PMCID PMC374335, DOI 10.1073/pnas.0306604101, lire en ligne, consulté le )
- McConnaughay, K.D.M. & Bazzaz, F.A. (1991) Is physical space a soil resource? Ecology, 72, 94–103.
- (en) Felix C.W. Loh, Jason C. Grabosky et Nina L. Bassuk, « Growth response of Ficus benjamina to limited soil volume and soil dilution in a skeletal soil container study », Urban Forestry & Urban Greening, vol. 2, no 1, , p. 53–62 (DOI 10.1078/1618-8667-00023, lire en ligne, consulté le )
- (en) Marina Semchenko, Michael J. Hutchings et Elizabeth A. John, « Challenging the tragedy of the commons in root competition: confounding effects of neighbour presence and substrate volume », Journal of Ecology, vol. 95, no 2, , p. 252–260 (DOI 10.1111/j.1365-2745.2007.01210.x, lire en ligne, consulté le )
- Feng Zhou, Aurélia Emonet, Valérie Dénervaud Tendon et Peter Marhavy, « Co-incidence of Damage and Microbial Patterns Controls Localized Immune Responses in Roots », Cell, vol. 180, no 3, , p. 440–453.e18 (ISSN 1097-4172, PMID 32032516, PMCID 7042715, DOI 10.1016/j.cell.2020.01.013, lire en ligne, consulté le )
- Jacques Lavabre et Vazken Andréassian, Eaux et forêts. La forêt, un outil de gestion des eaux ?, éditions Quae, , p. 83.
- Les enseignements s'appuient souvent sur des observations de plantes en germination, ce qui masque le fait que la plupart des poils absorbants des plantes adultes ne sont pas fonctionnels. Cette vision a longtemps prévalu chez les chercheurs en biologie végétale qui ont utilisé comme modèle expérimental des espèces exceptionnellement non mycorhiziennes, comme l'arabette (Arabidopsis thaliana, de la famille du chou)
- (en) Mika Tarkka, Uwe Nehls et Rüdiger Hampp, « Physiology of ectomycorrhiza (ECM) », Progress in Botany, vol. 66, , p. 247-276 (DOI 10.1007/3-540-27043-4_11)
- Marc-André Selosse, Jamais seul. Ces microbes qui construisent les plantes, les animaux et les civilisations, Éditions Actes Sud, , p. 171
- (en) M. M. Caldwell, J. H. Richards, « Hydraulic lift: water efflux from upper roots improves effectiveness of water uptake by deep roots », Oecologia, vol. 79, no 1, , p. 1–5 (DOI 10.1007/BF00378231).
- Michel-Claude Girard, Christian Walter, Jean-Claude Rémy, Jacques Berthelin, Jean-Louis Morel, Sols et environnement, Dunod, , p. 533.
- Les spéléologues observent l’eau ruisseler (issue de l'excédent de l'eau de pluie) le long des racines profondes.
- Ernst Zürcher, Les arbres, entre visible et invisible, Actes Sud Nature, , p. 193.
- (en) M.M. Caldwell, « Competition between root systems in natural communities », in Gregory P.J., Lake J.V. & Rose D.A. (eds.), Root development and function, Cambridge University Press, 1987, p. 167-185
- (en) J. Canadell, « Maximum rooting depth of vegetation types at the global scale », Oecologia, vol. 108, no 4, , p. 583–595 (DOI 10.1007/BF00329030, lire en ligne)
- (en) E. L. Stonea, « On the maximum extent of tree roots », Forest Ecology and Management, vol. 46, nos 1-2, , p. 59–102 (DOI 10.1016/0378-1127(91)90245-Q)
- Évelyne Samama, « Thaumatipoioi pharmackopôlai La singulière image des préparateurs et vendeurs de remèdes dans les textes grecs », dans Franck Collard, Évelyne Samama (dir.), Pharmacopoles et apothicaires, Les « pharmaciens » de l'Antiquité au Grand Siècle, L'Harmattan, (ISBN 2-296-01061-X)
- Florent Quellier, « Le concombre et quelques autres : périls et séduction », émission Concordance des temps sur France Culture, 16 juillet 2011
- Louis Joseph Marie Achille Goujon. Des bois propres aux constructions navales, manuel à l'usage des agents forestiers et maritimes. 1807. Lire en ligne
- Stål Ö. (1998) Interaction of tree roots and sewers. The Swedish experience. Arboriculture Journal Vol 22. N°4. November 1998. Arboricultural Association AB Academic Publishers
- (sv) [Orjan Stal Sverige Välkomna till VIÖS AB]
- Stål Ö. & Mattsson B. (1996), Alternative Methods to Avoid Operational and Maintenance Problems with Tree Roots in Storm Water Sewer Pipes. Integrated Water Management in Urban Areas.Searching for new realistic approaches with respect to developing world. Proceedings of the International Symposium held in Lund, Sweden, September 1995. Editor: J. Niemczynowicz. UNESCO - HIP. P 453-461
- Kaj Rolf et Orjan Stal (1994)
- Tree roots in sewer system in Malmo, Sweden ; Journal of Arboriculture 20(6): November 1994, p329-336
- D, Ridgers, K, Rolf and Ö, Stål (2006), Management and planning soulutions to lack of resistansnce to root penetration by modern PVC and Concrete Sewer. Arboricultural Journal 2006, Vol. 29, pp. 269–290
- D, Ridgers, K, Rolf and Ö, Stål. (2005), Management and planning solutions to modern PVC- and concrete sewer pipes' lack of re sistance to root penetration. Proceedings from Osnabrücker Baumpflegatage, 8 – 9 September 2005
- Stal, Orjan. (2001) The Interaction of Tree Roots and Sewers, City Trees, The Journal of the Society of Municipal Arborists , Volume 37, No. 4, July/August 2001
- Stal, Orjan. (2005), Swedish test show roots penetrate all kinds of joint pipes. In out, Inpipe News letter. Printed in Great Britain.
- STREP PLANTOID Project, voir aussi la vidéo Plantoid Project
Voir aussi
Bibliographie
- Christophe Drénou, Les racines : face cachée des arbres, Forêt privée française, , 335 p. (lire en ligne).
- Danjon F., Drénou C., Dupuy L., Lebourgeois F., 2007. « Le rôle du sol et de l'ancrage racinaire ». Landmann G., Birot Y. (Eds.). In: Forêt, Vent et Risque : des connaissances enrichies pour une meilleure gestion forestière. Éditions QUAE-ECOFOR, Versailles.
Radiographie
- Antoine Beauchamp, « Racines : vingt mille liens sous les terres », sur France Culture, .
Articles connexes
Liens externes
- Voir un schéma détaillé de : racines diverses.
- Structure et croissance de la racine, Université Pierre et Marie Curie.
- Animation Flash de la mise en place de la structure secondaire, Université Pierre et Marie Curie.
- Structure primaire des racines de dicotylédones.
- Database d'illustrations des structures/formes des plantes incluant collet et système racinaire, par espèce.
- Drawings of forest trees in the Root Systems Collection - WUR - Dessins de racines d'arbres en forêt, travail de l'université de Wageningue.