Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
| Cianeto de potássio Alerta sobre risco à saúde | |
|---|---|

| |
| |
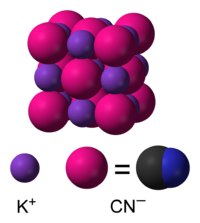
| Nome IUPAC | Cianeto de potássio |
| Outros nomes | Cianureto (de potássio) |
| Identificadores | |
| Número CAS | |
| Número EINECS | |
| Número RTECS | TS8750000 |
| Propriedades | |
| Fórmula molecular | KCN |
| Massa molar | 65.12 g/mol |
| Aparência | Sólido cristalino incolor deliquescente |
| Densidade | 1.52 g/cm3 |
| Ponto de fusão |
634.5 °C |
| Ponto de ebulição |
1625 °C |
| Solubilidade em água | 71.6 g/100 ml (25 °C) 100 g/100 mL (100 °C) |
| Solubilidade em metanol | 4.9 g/100 mL (20 °C) |
| Solubilidade em glicerol | solúvel |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
−131.5 kJ/mol |
| Entropia molar padrão S |
127.8 J K−1 mol−1 |
| Riscos associados | |
| MSDS | ICSC 0671 |
| Classificação UE | Muito tóxico (T+) Perigoso para o meio ambiente (N) |
| Índice UE | 006-007-00-5 |
| NFPA 704 | |
| Frases R | R26/27/28, R32, R35 |
| Frases S | S1/2, S7, S28, S29, S45, S60, S61 |
| Ponto de fulgor | Não inflamável |
| LD50 | 5–10 mg/kg (oral em ratos, camundongos, coelhos)[1] |
| Compostos relacionados | |
| Outros aniões/ânions | Cianato de potássio Tiocianato de potássio |
| Outros catiões/cátions | Cianeto de sódio |
| Compostos relacionados | Cianeto de hidrogênio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Cianeto de Potássio ou Cianureto de potássio é um composto químico altamente tóxico. Na verdade é o íon cianeto (CN) que causa a intoxicação, pois torna inerte a Citocromo c oxidase, impedindo a respiração celular, o que por sua vez acarreta em uma morte rápida. A LD50 = 2.500 a 5.000 mg (2,5 a 5g). Soldados alemães da Segunda Guerra Mundial capturados usavam-no para cometer suicídio através de ingestão, assim como utilizado no suicídio coletivo de Jonestown.
Deve-se ter extremo cuidado ao manipular esse composto, pois o contato com qualquer ácido converte esse composto ao ácido cianídrico (HCN), um composto letal. Tanto o cianeto de potássio quanto o ácido cianídrico são consideradas substâncias hematóxicas (que intoxicam o sangue), posto que o ácido cianídrico foi usado como arma química pelos alemães além de cloro gasoso e fosgênio.

KCN é produzido ao combinar cianeto de hidrogênio com hidróxido de potássio[2].
Aproximadamente 50,000 toneladas são produzidas anualmente (a produção de cianeto de sódio é 10x esta quantidade). É eliminado mais eficientemente com peróxido de hidrogênio:[2]