Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
| Borneol | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
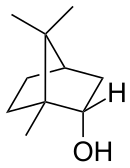
| ||||
Structuurformule van borneol
| ||||

| ||||
Molecuulmodel van borneol
| ||||
| Algemeen | ||||
| Molecuulformule | C10H18O | |||
| IUPAC-naam | endo-1,7,7-trimethylbicyclo[2.2.1]heptan-2-ol | |||
| Andere namen | kamfol, 2-hydroxykamfaan, 2-hydroxybornaan | |||
| Molmassa | 154,24932 g/mol | |||
| SMILES | CC1(C2CCC1(C(C2)O)C)C
| |||
| InChI | 1S/C10H18O/c1-9(2)7-4-5-10(9,3)8(11)6-7/h7-8,11H,4-6H2,1-3H3/t7-,8+,10+/m1/s1
| |||
| CAS-nummer | 464-43-7 | |||
| EG-nummer | 208-080-0 | |||
| PubChem | 6552009 | |||
| Wikidata | Q412435 | |||
| Beschrijving | Kleurloze kristallen | |||
| Vergelijkbaar met | kamfer | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H228 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P210 | |||
| VN-nummer | 1312 | |||
| ADR-klasse | Gevarenklasse 4.1 | |||
| LD50 (ratten) | (oraal) 5033 mg/kg | |||
| LD50 (muizen) | (oraal) 1750 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,011 g/cm³ | |||
| Smeltpunt | 208 °C | |||
| Kookpunt | 213 °C | |||
| Vlampunt | 65 °C | |||
| Onoplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Borneol of kamfol is een gebrugde organische verbinding met als brutoformule C10H18O. De stof komt voor als kleurloze en naar kamfer ruikende kristallen, die onoplosbaar zijn in water.
Borneol is structureel gezien sterk verwant met bornaan en kamfer. Er bestaat een exo-isomeer van borneol: isoborneol. Hierbij is de hydroxylgroep exo geplaatst ten opzichte van de ringstructuur. Bij borneol staat de hydroxylgroep endo geplaatst. Borneol en isoborneol zijn geen spiegelbeeld van elkaar en dus ook geen enantiomeren.
Borneol behoort tot de klasse der bicyclische terpenen (meer bepaald de monoterpenen) en vormt daarom een component van een groot aantal essentiële oliën. Het is tevens een secundair alcohol.
Borneol kan eenvoudig met salpeterzuur of chroomzuur geoxideerd worden tot de ketonvorm kamfer. Omgekeerd kan kamfer gereduceerd worden tot borneol door middel van een Meerwein-Ponndorf-Verley-reductie. Isoborneol kan worden gevormd door de irreversibele reductie van kamfer met natriumboorhydride:
Borneol komt in de natuur voor als het optisch actieve d-(+)-borneol. Het kan worden aangetroffen bij verschillende soorten uit het geslacht Artemisia, uit de familie Dipterocarpaceae en bij de soorten Blumea balsamifera en Kaempferia galanga. Verder komt het in mindere mate voor in etherische oliën van koriander, boerenwormkruid, nootmuskaat, salie en rozemarijn.
Borneol is een relatief stabiele verbinding, maar kan schadelijk en irriterend zijn voor ogen, huid en luchtwegen. De verbinding is niet direct toxisch, maar in grote hoeveelheden kan het wel schadelijk zijn. Borneol is licht ontvlambaar en moet daarom ver verwijderd blijven van iedere vorm van vuur of vonken.