Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
| Radioterapia | |
|---|---|
Procedura medica 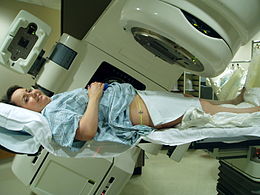 Una paziente si sottopone a radioterapia alla pelvi | |
| Classificazione e risorse esterne | |
| MeSH | D011878 |
| MedlinePlus | 001918 |
La radioterapia è una disciplina medica consistente nell'utilizzo di radiazioni ionizzanti. La radioterapia è utilizzata soprattutto nel trattamento di forme di tumore, infatti utilizza un fascio di fotoni penetranti, di 5-10 MeV di energia, per danneggiare il patrimonio genetico delle cellule malate e impedire così che proliferino[1], mentre è poco impiegata in patologie non oncologiche. La radioterapia può essere curativa in un certo numero di tipi di cancro, se confinati in una zona del corpo sulla base della classificazione TNM della lesione stessa.
È prassi comune combinare la radioterapia con la chirurgia, con la chemioterapia, con l'ormonoterapia e l'immunoterapia. Lo scopo esatto del trattamento (curativo-radicale, adiuvante, neoadiuvante, terapeutico o palliativo) dipenderà dal tipo di tumore, dalla posizione e stadio, nonché dalla salute generale del paziente.
Le radiazioni ionizzanti utilizzate in radioterapia sono in grado di danneggiare il DNA del tessuto bersaglio. Le cellule tumorali sono, in genere, scarsamente capaci di riparare i propri danni e quindi vanno incontro a morte cellulare per apoptosi. Per risparmiare tessuti sani, ad esempio pelle o organi che la radiazione deve superare per arrivare al tumore, i fasci delle radiazioni vengono sagomati e rivolti da diverse angolazioni, intersecandosi nel centro della zona da trattare, dove perciò vi sarà un quantitativo di dose assorbita totale superiore che nelle parti adiacenti.
Oltre al tumore stesso, i campi di radiazione possono comprendere anche i linfonodi drenanti se sono clinicamente o radiologicamente coinvolti con il tumore, o se si ritiene che possa esserci un rischio di diffusione maligna. È necessario includere un margine di tessuto sano circostante il tumore per consentire le incertezze dovute al posizionamento e al movimento interno degli organi.
L'irradiazione corporea totale (TBI) è una tecnica radioterapica utilizzata per preparare il corpo per ricevere un trapianto di midollo osseo. La brachiterapia, in cui una sorgente di radiazione è posizionata all'interno o vicino alla zona da trattare, è un'altra forma di radioterapia che minimizza l'esposizione del tessuto sano durante le procedure per curare i tumori della mammella, prostata e altri organi.

La medicina utilizza la radioterapia come trattamento per il cancro da più di 100 anni, con le sue prime radici tracciate dalla scoperta dei raggi X nel 1895 da Wilhelm Röntgen[2]. Emil Grubbe di Chicago è stato forse il primo medico statunitense ad utilizzare raggi x per curare il cancro, a partire dal 1896[3].
Il campo della radioterapia ha cominciato a crescere nella prima parte del 1900, ciò è stato gran parte dovuto al lavoro pionieristico della scienziata vincitrice del premio Nobel, Marie Curie (1867-1934), che scoprì la radioattività degli elementi, polonio e radio, nel 1898. In questo modo ha inizio una nuova era nel trattamento medico e della ricerca[2]. Uno dei primi congressi di elettrologia e radiologia medica fu quello svoltosi in Italia nel 1906.[4] Il radio è stato utilizzato in varie forme fino alla metà del 1900, quando la telecobaltoterapia e le unità di cesio hanno iniziato ad usare tale elemento. Infine, gli acceleratori lineari medici sono stati utilizzati come sorgenti di radiazioni dalla fine del 1940.
Con l'invenzione di Godfrey Hounsfield della tomografia computerizzata (CT) nel 1971, la progettazione tridimensionale è diventata una possibilità e ha creato un passaggio da 2D a 3D per la distribuzione della radiazione. La pianificazione basata sulla CT permette ai medici di determinare con maggiore precisione la distribuzione della dose di radiazione, utilizzando immagini tomografiche assiali dell'anatomia del paziente. Le unità di ortovoltaggio e di cobalto sono state in gran parte sostituite da acceleratori lineari a megavoltaggio,

utili per le loro energie penetranti e per la mancanza di sorgenti fisiche di radiazione.
L'avvento di nuove tecnologie della diagnostica per immagini, comprese la risonanza magnetica (MRI) nel 1970 e la tomografia ad emissione di positroni (PET) nel 1980, hanno portato il trattamento dalla radioterapia conformazionale tridimensionale (3D) alla radioterapia a intensità modulata (IMRT), alla radioterapia guidata dalle immagini (IGRT) e alla tomoterapia. Questi progressi che hanno permesso agli oncologi di radiazione di vedere e colpire meglio i tumori, hanno portato a migliori risultati nel trattamento, con una maggiore conservazione dell'organo e meno effetti collaterali[5].

La radioterapia come disciplina medica, è rivolta principalmente al trattamento dei tumori.
La radioterapia (da sola o in combinazione con la chirurgia e/o la chemioterapia) è uno strumento efficace per il controllo locale dei tumori. Si calcola che circa 1300-1800 pazienti all'anno ogni 750.000 necessitino di un ricorso alla radioterapia.[6]
Si tratta di una pratica medica decisamente consolidata e di comprovata efficacia, ma che ha controindicazioni nei potenziali pericoli dovuti all'impiego delle stesse radiazioni ionizzanti, nei possibili danni da radiazioni e nella probabilità che le stesse inducano l'insorgenza di secondi tumori.
Il meccanismo di interazione tra il fascio di fotoni sfruttati dalla radioterapia e le cellule malate è il seguente: i fotoni dei raggi X colpiscono gli elettroni dei tessuti e li mettono in movimento, questi elettroni “secondari” percorrono zigzagando uno o due centimetri nei tessuti e ionizzano gli atomi delle molecole di DNA nelle cellule che incontrano, disinnescando così il funzionamento dei loro geni.[1]
Due importanti modalità radioterapeutiche sono la TBI e la TSEBI.
La radiazione corporea totale (Total Body Irradiation - TBI), è l'irradiazione totale e simultanea del corpo (in una o più frazioni) utilizzando fasci di fotoni ad alta energia. Consiste in una particolare tecnica radioterapica utilizzata per preparare il paziente a ricevere un trapianto di midollo osseo (TMO o BMT). A seconda delle necessità, questo tipo di intervento può essere eseguito con somministrazioni del tipo high dose, low dose o very low dose. Nello specifico le finalità di questo trattamento sono due: sopprimere il sistema immunitario per prevenire il rigetto del midollo del donatore familiare o non familiare, eradicare le cellule neoplastiche che residuano ai trattamenti chemioterapici.[7]
Con TSEBI, Total Skin Electron Beam Irradiation, è indicata l'irradiazione cutanea totale effettuata con fasci di elettroni[8]. Si tratta di una terapia impiegata nel caso di neoplasie cutanee diffuse o in pazienti affetti da micosi fungoide.
Esiste anche una radioterapia non oncologica, impiegata nel trattamento di situazioni non oncologiche presenti più frequentemente, ma non esclusivamente, in Geriatria.
La radioterapia si basa sul principio d'indirizzare la radiazione ionizzante sulle cellule cancerogene per danneggiarne il DNA. Mentre le cellule sane dispongono di meccanismi atti a riparare i danni che possono avvenire sul loro DNA, le cellule cancerogene dispongono di meccanismi molto meno efficienti, per cui un danno è più facilmente letale per questo tipo di cellula. Le radiazioni ionizzanti generano nelle cellule radicali liberi, che danneggiano il patrimonio genetico della cellula ospite non in grado di opporvisi.
La principale limitazione nell'uso di questa tecnica consiste nel fatto che le cellule di tumori solidi risultano essere in debito di ossigeno (ipossia) e questo le rende tanto più resistenti alle radiazioni quanto minore è la presenza di ossigeno. L'ossigeno contribuisce a rendere meno riparabile il danno biologico causato dai radicali liberi generati dalle ionizzazioni, e interagisce con gli atomi di idrogeno H+ liberi creando ossidanti OHx: questo inibisce la reazione di ritorno che altrimenti si avrebbe (da Hx+OHx ad H2O).
Tale effetto è più marcato nelle radiazioni a bassa energia (linear energy transfer elevato), tanto che in presenza di ossigeno l'efficacia biologica di tali radiazioni è aumentata di 3 volte.
Sono in sperimentazione tecniche per aumentare l'ossigenazione in fase di trattamento radioterapico, o diminuire l'ossigeno nei tessuti sani antistanti i tumori per limitarne il danno biologico.
La radioterapia è principalmente indicata per il trattamento di neoplasie. In misura minore, viene usata per patologie non tumorali che si giovano dagli effetti indotti dalle radiazioni, come nel caso di esoftalmo endocrino, nella prevenzione dei cheloidi, nella prevenzione delle ossificazioni eterotopiche o come nel trattamento di malformazioni artero-venose intracraniche.
Nel trattamento dei tumori, la radioterapia si prefigge di ottenere la totale distruzione di una neoplasia, senza indurre alterazioni gravi e irreversibili ai tessuti circostanti. Per garantire questo risultato, massimizzando l'intervento nell'area interessata e minimizzando l'esposizione delle zone circostanti, è talora utile utilizzare differenti tipi di radiazioni, sia fotoniche (raggi X o raggi γ) che corpuscolari (elettroni, raggi alfa, protoni, ioni carbonio, ecc.) differentemente distribuite sulla sede neoplastica.
Circa non gli effetti non terapeutici, ma i possibili legami causa-effetto fra la radiazione ionizzante e cancro, utile visionare gli effetti collaterali e la sezione radioprotezione.
In un approccio multidisciplinare (e talora anche multi – istituzionale), che comporta anche controlli ematologici, per quanto riguarda le tecniche radioterapiche dei vari organi ed apparati della anatomia umana, il trattamento radioterapico di una neoplasia coinvolge diverse figure specialistiche:

Fra le procedure programmate sulle macchine di radioterapia vi sono la taratura dei sistemi dosimetrici e la calibrazione dei fasci di terapia.
La prima fase della procedura relativa al paziente consiste invece in un suo posizionamento e negli accorgimenti atti a mantenere la riproducibilità di appositi e comodi accessori di immobilizzazione.
Dette apparecchiature per posizionamento e contenzione del paziente sono solitamente site nell'area cosiddetta "di simulazione".
Si può poi, nel caso, effettuare una pre-simulazione rx; possono essere eseguite registrazioni e fusioni di immagini multimodali; comunque si passa generalmente all'utilizzo della tomografia assiale con l'impiego contemporaneamente di appositi laser che consentono di identificare corrette coordinate di centraggio, e vengono lasciati opportuni reperti. L'uso della tomografia assiale con gli appositi laser, serve per le DRR (o radiografie digitali ricostruite), in particolare per poter ricostruire un'immagine tridimensionale dell'area di trattamento; vengono quindi identificate possibili situazioni di criticità e/o di particolare rilevanza clinica ed anche utilizzati eventuali speciali markers ed è possibile effettuare una post-simulazione rx di controllo.
Con questi dati viene steso un TPS , ovvero Treatment Planning System, che identifica le zone da irradiare e gli OAR (Organs At Risk, organi da non irradiare o risparmiare), e da cui si desumono le curve di isodose bidimensionali e ricostruzioni bidimensionali e tridimensionali oltre agli istogrammi Dose-Volume e le visualizzazioni BEV (Beam Eye View) e REV (Room Eye View).
Le principali tecniche radioterapiche (tranne che per IORT, curieterapia e radioterapia metabolica), per essere eseguite, necessitano di sistemi di localizzazione e controllo, ottenuti con pellicole fotografiche che registrano il posizionamento prima o durante il trattamento ("radiotherapy localization and verification"). I tipi di 'portal radiograph' (appropriate pellicole inserite in apposite cassette) sono differenti: le localization, quando l'immagine è acquisita mediante una pellicola 'veloce' esposta per pochi secondi prima di effettuare il trattamento (radiografia di localizzazione); le verification, quando l'immagine è acquisita da una pellicola "lenta" esposta al fascio radiante per tutta la durata della seduta (radiografia di verifica). Da ricordare le portal radiograph "a doppia esposizione" quando l'immagine è acquisita da una pellicola 'veloce' sottoposta a due esposizioni sequenziali di cui la prima corrisponde al campo trattato mentre la seconda a un campo più ampio del primo; ottenute con esposizione di pochi secondi hanno la funzione di rendere fattibile in modo semplice il confronto tra il campo di trattamento e le strutture anatomiche vicine. Ha costituito un valido strumento alternativo ai portal film la modalità di controllo di tipo radioscopico denominato Electronic Portal Imaging Device (EPID), costituita da un braccio meccanico mobile situato sotto la testata dell'acceleratore e con sistema che acquisisce immagini, di seguito elaborate e visualizzate tramite una ‘'workstation’'.
La radioterapia esterna a fascio collimato si fonda sull'utilizzo di un fascio di radiazioni prodotte da sorgenti situate all'esterno del paziente e viene utilizzata sia con radiazioni fotoniche sia con l'utilizzo di elettroni veloci.
A seconda del loro potenziale gli acceleratori lineari (che sono spesso ‘Dual Energy’: 4 MV, 6-18 MV 6-15 MV, 6-10 MV) possono produrre anche elettroni di diversi livelli energetici (MeV). Gli elettroni hanno una modalità di diffusione della dose differente da quella dei raggi X, poiché data la massima dose ad una profondità che dipende dalla loro energia, la dose va poi molto velocemente a pressoché zero e dunque vengono utilizzati per irradiare tessuti più superficiali, risparmiando quelli più profondi.

Se si escludono la TBI e la meno frequente TSEBI, considerando le diverse tecniche impiegate per il numero dei pazienti, e circa tre "campi" per paziente, il tempo medio di trattamento per paziente, inteso come la durata di permanenza nel "bunker" (sempre sotto osservazione "visiva-televisiva" e con continua possibilità dello scambiarsi comunicazioni), è di 15 minuti e comunque non inferiore ai 10 minuti.
I giorni totali dei trattamenti più frequenti sono: 1, 5, 10, 13, 15, 18, 23, 25, 27, 30, 35, 38; per trattamenti palliativi e radicali.
Protoni, neutroni e ioni carbonio vengono invece impiegati per l'adroterapia. Il nome adroterapia deriva da terapia adronica, si tratta di una terapia che utilizza fasci di adroni, particelle caratterizzate dall'interazione forte. Il vantaggio del loro utilizzo consiste nella capacità di depositare alte dosi di radiazioni nel tumore limitando al massimo le dosi agli organi critici, anche quando questi si trovano molto vicini al 'bersaglio'. Prevede l'utilizzo di un ciclotrone per accelerare le particelle a velocità elevate, impossibili da raggiungere con acceleratori di tipo lineare. Gli ioni di carbonio utilizzati hanno una efficacia biologica superiore ai raggi X ed anche ai protoni.
Non rientrano nella definizione di ‘radioterapia esterna’ la brachiterapia e la radioterapia metabolica, di seguito descritte.
La brachiterapia (o curieterapia) fino ad ora impiegata può essere classificata come low-dose rate (LDR), medium-dose rate (MDR), high-dose rate (HDR) e pulsed-dose rate (PDR).
Gli isotopi maggiormente usati sono: iridio 192, iodio 125, stronzio 89, cesio 137, palladio 103, oro 198.
La radioterapia può essere fatta pertanto anche con radionuclidi in tecniche apparentate con la medicina nucleare, per esempio la radioterapia della tiroide con Iodio-131, o quella con stronzio, samario o renio per le metastasi ossee. Da menzionare anche tecniche di radioembolizzazione e la radioterapia recettoriale (ad esempio con ittrio-90).
L'intensità di dose, definita come la dose ricevuta nell'unità di tempo, è chiamata meglio tasso di dose[9]; in ogni caso assume importanza notevole, rispetto alla maggioranza dei trattamenti, il frazionamento. Il trattamento radiante esterno è infatti abitualmente non continuo, ma frazionato e viene eseguito seguendo due principali schemi di frazionamento (o somministrazione) della dose:
A tasso e frazionamento di dose, volume irradiato e dose totale erogata sono in parte correlabili la tossicità e controllo locale dei trattamenti radioterapici con ottimizzazione dosimetrica e radiobiologica.
Il metodo di somministrare dosi piccole e frequenti è utilizzato specie quando utile a permettere alle cellule e ai tessuti sani di riparare i danni indotti dalle radiazioni, senza alterare l'efficacia sul tumore.
La radioterapia, come del resto la farmacoterapia, ha ovviamente effetti biologici e la dose totale, erogata ed assorbita, è importante anche in relazione al frazionamento scelto (che si correla al concetto di dose somministrata nel tempo). Il frazionamento come già espresso è suddivisibile in convenzionale e ipofrazionato (non più di una frazione al giorno) ed iperfrazionato (più di una frazione al giorno).
La somministrazione dell'irradiazione esterna, convenzionalmente, è una volta al giorno per 5 giorni consecutivi per una dose settimanale di 9-10 Gray = Gy (comunque non inferiore a circa 7,75 Gy e non superiore a circa 11,85 Gy, ovvero 775-900-1000-1185 centigray = cGy). La dose per frazione giornaliera (1 Gy = 100 cGy) è, non considerando un megafrazionamento, usualmente di:
Generalmente l'irradiazione esterna viene dunque effettuata giornalmente (per un massimo di 5 frazioni settimanali) e la dose varia in relazione agli intenti (radicali/sintomatico-palliativi), al tipo di tumore, all'affiancamento ad essa di altre terapie quali la chemioterapia, la chirurgia o l'utilizzo di altre modalità. Nei casi di trattamenti radicali (in cui si vuole eradicare il tumore), la dose totale tipica fornita ai tumori epiteliali solidi varia dai 46-50-54 ai 60-70 Gray (Gy) o più; per i linfomi le dosi sono comprese fra 20-32,5 e 45 Gy.
Spesso la radioterapia, senza chemioterapia oppure integrata alla chemioterapia (radiochemioterapia), va inquadrata secondo altre terapie: o come trattamento "singolo" o come trattamento precauzionale di "consolidamento post chemio" nei linfomi, oppure, nei tumori 'solidi', come trattamento quando inoperabili, (es. cancro della vescica localmente avanzato), o per poter facilitare l'operazione e ridurre i rischi al paziente o per rendere l'intervento meno mutilante, (es.adenocarcinoma del retto), o per migliorare il risultato terapeutico (es.cancro dell'esofago). La radioterapia è in grado anche di consentire la conservazione o la preservazione d'organo oppure una minor mutilazione d'organo.
La radioterapia può essere classificata come:
Oltre che con la chirurgia, molto spesso la radioterapia viene associata a trattamenti di chemioterapia con antineoplastici. In questi ultimi anni, si sta inoltre affermando come valida associazione alla radioterapia, il trattamento di ipertermia oncologica. Tale terapia, riconosciuta dal sistema sanitario nazionale italiano (codice prontuario 9985.2), risulta in un potenziamento dell'effetto della radioterapia consentendo la riduzione delle dosi di radiazioni alle quali si deve sottoporre il paziente con evidenti benefici in termini di riduzione degli effetti collaterali. La radioterapia viene anche combinata con immunoterapia e con terapia con anticorpi monoclonali.
La radiobiologia è una branca delle scienze bio-mediche, che studia gli effetti provocati dalle radiazioni quando esse interagiscono con un sistema biologico (sole, o in associazione).
Essa ha diversi campi applicativi, correlati all'impiego delle radiazioni ionizzanti e non ionizzanti, quali la vecchia radioterapia non oncologica, la radioprotezionistica, l'imaging, e particolarmente l'oncologia clinico-radioterapeutica e radiochemioterapica.
Per la valutazione delle radiazioni ionizzanti l'unità di misura più utilizzata è il gray, cioè la dose di energia assorbita per unità di massa. Il LET, l'Energia Lineare di Trasferimento, è l'energia rilasciata dalla radiazione per unità di lunghezza. Per quanto riguarda i tessuti biologici (specie dal punto di vista radioprotezionistico), si può parlare di dose equivalente e di dose efficace. Qui l'unità di misura è il Sievert (Sv). La dose equivalente viene calcolata moltiplicando la dose assorbita per un fattore di peso che dipende dal tipo di radiazione. La dose efficace rappresenta la sommatoria delle dosi equivalenti; sommatoria moltiplicata per un fattore di ponderazione tissutale, ovvero per pesi relativi ai vari organi e tessuti; questi ultimi pesi tengono conto della diversa sensibilità alle radiazioni degli organi e dei tessuti irradiati.
Tecnica atta a ridurre la dispersione delle radiazioni, ed a ridurne gli effetti collaterali.
La radioterapia è un metodo di cura praticamente indolore di per sé. Nei casi in cui vengano utilizzati trattamenti palliativi risulta inoltre avere anche effetti collaterali minimi (ad esempio, modeste irritazioni cutanee della zona 'bombardata'). Nei casi in cui invece vengano utilizzati trattamenti radicali si possono indurre vari tipi di effetti collaterali che si manifestano durante o nelle settimane successive il trattamento stesso (effetti collaterali di tipo precoce) oppure nei mesi o anni direttamente successivi al trattamento (effetti collaterali di tipo tardivo). Uno di questi effetti collaterali è la fibrosi, un indurimento dei tessuti e delle ghiandole linfatiche nella zona sottoposta a trattamento radiante.
La natura degli effetti collaterali dipende dall'organo trattato, da frazionamento, tasso di dose, tempo totale di trattamento, intervalli nel trattamento, volume irradiato, tipo di tecnica utilizzata. Ogni individuo può presentare delle reazioni proprie, rispetto alla quantità di dose assorbita; inoltre trattamenti successivi su stessi siti trattati in precedenza possono causare particolari problemi: ogni tessuto presenta una tolleranza massima alla radiazione, quindi trattare in periodi diversi dei tessuti, organi o apparati che hanno ricevuto la massima dose anche anni prima può causare vari problemi come effetti collaterali a lungo termine anche a distanza di diversi anni.
Una volta escluse grazie ad apposite e rigorose procedure osservazionali e preventive le possibilità di incidenti, uno degli obiettivi principali della moderna radioterapia è quello di ridurre al minimo gli effetti collaterali, e di aiutare i pazienti a capire e accettare quegli effetti collaterali che non sono eliminabili. Gli effetti collaterali si dividono in acuti e cronici; vi sono state nel tempo diverse definizioni, da diversi autori, circa quando definire acuti o cronici gli effetti collaterali. Si sono definite complicanze immediate quelle entro il primo giorno; danni acuti quelli a partire dal primo giorno successivo all'inizio del trattamento e fino a 180 giorni; danni tardivi o cronici quelli dopo 180 giorni. Effetti collaterali tardivi o cronici sono stati definiti da altri quelli che si verificavano dopo 90 giorni dall'inizio del trattamento ed ancora quelli comparsi 90 giorni dopo la fine del trattamento o quelli non guariti entro 90 giorni dalla fine del trattamento. Dopo lo scritto di Bentzen SM, Overgaard J.,(Clinical manifestations of normal-tissue damage), del 1997, il cut-off più utilizzato per distinguerli sono i 3 mesi (acuti nei primi tre mesi post-trattamento, cronici dopo i tre mesi dal trattamento).
Molti effetti collaterali sono previsti ed attesi. Vi è stata comunque una evoluzione della loro identificazione basata sull'osservazione clinica con follow-up sempre maggiore, correlabile anche con lo svilupparsi delle apparecchiature e delle tecniche di radioterapia e con la modellistica radio-biologica interpretativa, descrittiva e previsionale, (a partire dai modelli utilizzanti un formalismo del modello LQ e nei quali un alfa/beta di 3 è tipico per gli effetti collaterali cronici ed un alfa/beta di 10 è invece tipico per gli effetti collaterali acuti come anche per il controllo tumorale), ma soprattutto sugli studi anatomopatologici e fisiologici.
Di conseguenza ne sono derivate varie classificazioni, le principali delle quali sono dovute a:
Le classificazioni che più si sono affermate sono dunque:
Questi effetti possono risultare anche minimi, e dipendono dal tessuto che riceve il trattamento:
| Controllo di autorità | Thesaurus BNCF 23636 · LCCN (EN) sh00005896 · GND (DE) 4057833-1 · BNF (FR) cb11941666h (data) · J9U (EN, HE) 987007560616505171 · NDL (EN, JA) 00563532 |
|---|