Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
42Mo Molibdenum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Fragmen kristal dan kubus molibdenum 1 cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
Garis spektrum molibdenum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /molibdènum/[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | metalik abu-abu | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molibdenum dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 42 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-d | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | logam transisi | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Kr] 5s1 4d5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 13, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 2896 K (2623 °C, 4753 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 4912 K (4639 °C, 8382 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 10,28 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 9,33 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 37,48 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 598 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 24,06 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | −4, −2, −1, 0, +1,[2] +2, +3, +4, +5, +6 (oksida asam kuat) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 2,16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 684,3 kJ/mol ke-2: 1560 kJ/mol ke-3: 2618 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 139 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 154±5 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat badan (bcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 5400 m/s (pada s.k.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 4,8 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 138 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Difusivitas termal | 54,3 mm2/s (suhu 300 K)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 53,4 nΩ·m (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | +89,0×10−6 cm3/mol (298 K)[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 329 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 126 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 230 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,31 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Vickers | 1400–2740 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 1370–2500 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7439-98-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan | Carl W. Scheele (1778) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isolasi pertama | Peter J. Hjelm (1781) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop molibdenum yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Molibdenum adalah unsur kimia dengan lambang Mo dan nomor atom 42. Namanya diambil dari Neo-Latin molybdaenum, dari bahasa Yunani Kuno Μόλυβδος molybdos, yang berarti timbal, karena bijihnya dirancukan dengan bijih timbal.[5] Mineral molibdenum telah dikenal sepanjang sejarah, tetapi unsurnya ditemukan (dalam arti membedakannya sebagai entitas baru dari garam mineral logam lainnya) pada tahun 1778 oleh Carl Wilhelm Scheele. Logamnya pertama kali diisolasi pada tahun 1781 oleh Peter Jacob Hjelm.
Molibdenum tidak terjadi secara alami sebagai logam bebas di Bumi; ia hanya ditemukan dalam berbagai tingkat oksidasi pada mineral. Unsur bebasnya, suatu logam keperakan dengan noda abu-abu, memiliki titik lebur ke-6 di antara semua unsur. Ia mudah membentuk karbida stabil dan keras dalam logam paduan, dan untuk alasan ini, sebagian besar produksi dunia unsur ini (sekitar 80%) digunakan dalam paduan baja, termasuk paduan berkekuatan tinggi dan superalloy.
Sebagian besar senyawa molibdenum memiliki kelarutan rendah dalam air, tetapi ketika mineral molibdenum terkena oksigen dan air, ion molibdat MoO yang dihasilkan cukup larut. Dalam skala industri, senyawa molibdenum (sekitar 14% dari produksi dunia) digunakan dalam aplikasi tekanan tinggi dan suhu tinggi sebagai pigmen dan katalis.
Enzim pengikat molibdenum sejauh ini merupakan katalis bakteri yang paling umum untuk memutus ikatan kimia dalam molekul nitrogen atmosfer dalam proses fiksasi nitrogen. Setidaknya 50 enzim molibdenum sekarang dikenal pada bakteri dan hewan, walaupun hanya enzim bakteri dan sianobakteria yang terlibat dalam fiksasi nitrogen. Nitrogenase ini mengandung molibdenum dalam bentuk yang berbeda dari enzim molibdenum lainnya, yang semuanya mengandung molibdenum teroksidasi penuh dalam kofaktor molibdenum. Berbagai enzim kofaktor molibdenum ini sangat penting bagi organisme, dan molibdenum adalah unsur esensial untuk kehidupan di semua organisme eukariota yang lebih tinggi, meskipun tidak pada semua bakteri.
Dalam bentuknya yang murni, molibdenum adalah logam abu-abu keperakan dengan kekerasan Mohs sebesar 5,5. Mo memiliki titik lebur 2.623 °C (4.753 °F; 2.896 K); dari unsur alami, hanya tantalum, osmium, renium, wolfram, dan karbon yang memiliki titik lebur lebih tinggi.[5] Oksidasi lemah molibdenum dimulai pada 300 °C (572 °F; 573 K). Ia salah satu yang memiliki koefisien ekspansi termal terendah di antara logam yang digunakan secara komersial.[6] Kekuatan tarik kabel molibdenum meningkat sekitar 3 kali, dari sekitar 10 menjadi 30 GPa, ketika diameternya menurun dari ~50-100 nm ke 10 nm.[7]
Terdapat 35 isotop molibdenum yang diketahui, dengan kisaran massa atom antara 83 sampai 117, dan juga empat isomer nuklir metastabil. Tujuh isotop terjadi secara alami, dengan massa atom 92, 94, 95, 96, 97, 98, dan 100. Dari isotop alami ini, hanya molibdenum-100 yang tidak stabil.[8]
Molibdenum-98 adalah isotop paling melimpah, yang menyusun 24,14% dari semua molibdenum. Molibdenum-100 memiliki waktu paruh sekitar 1019 tahun dan mengalami peluruhan beta ganda menjadi rutenium-100. Isotop molibdenum dengan nomor massa 111 sampai 117 semuanya memiliki waktu paruh sekitar 150 ns.[8][9] Semua isotop molibdenum yang tidak stabil meluruh menjadi isotop niobium, teknesium, dan rutenium.[9]
Seperti yang juga dicatat di bawah, aplikasi molibdenum isotopik yang paling umum melibatkan molibdenum-99, yang merupakan produk fisi. Ini adalah radioisotop induk untuk radioisotop anak yang memancarkan gamma dan berumur pendek teknesium-99m, sebuah isomer nuklir yang digunakan dalam berbagai aplikasi pencitraan dalam bidang kedokteran.[10] Pada tahun 2008, Delft University of Technology mengajukan permohonan paten untuk produksi molibdenum-99 berbasis molibdenum-98.[11]
| Tingkat oksidasi |
Contoh[12] |
|---|---|
| −2 | Na2[Mo2(CO)10] |
| 0 | Mo(CO)6 |
| +1 | Na[C6H6Mo] |
| +2 | MoCl2 |
| +3 | Na3[Mo(CN)]6 |
| +4 | MoS2 |
| +5 | MoCl5 |
| +6 | MoF6 |

Molibdenum adalah logam transisi dengan elektronegativitas 2,16 pada skala Pauling dan bobot atom standar 95,95 g/mol.[13][14] Ia tidak tampak bereaksi dengan oksigen atau air pada suhu kamar, dan oksidasi ruah terjadi pada suhu di atas 600 °C, menghasilkan molibdenum trioksida:
Trioksidanya volatil dan menyublim pada suhu tinggi. Ini mencegah pembentukan lapisan oksida pelindung (pemasif) yang terus menerus, yang akan menghentikan oksidasi logam ruah.[15] Molibdenum memiliki beberapa tingkat oksidasi, yang paling stabil adalah +4 dan +6 (dicetak tebal pada tabel di sebelah kiri). Kimia dan senyawa menunjukkan kemiripan yang lebih mirip wolfram dibanding kromium; ketidakstabilan senyawa molibdenum(III) dan wolfram(III), misalnya, kontras dengan kestabilan senyawa kromium(III). Keadaan oksidasi tertinggi terlihat pada molibdenum(VI) oksida (MoO3), sedangkan senyawa sulfur normal adalah molibdenum disulfida MoS2.[16]
Molibdenum(VI) oksida larut dalam basa kuat, membentuk molibdat (MoO2−4). Molibdat adalah oksidator yang lebih lemah daripada kromat, tetapi menunjukkan kecenderungan yang sama untuk membentuk kompleks oksionion dengan kondensasi pada nilai pH yang lebih rendah, seperti [Mo''"; dan [Mo''";. Polimolibdat dapat bergabung dengan ion lain, membentuk polioksometalat.[17] Heteropolimolibdat yang mengandung fosfor berwarna biru tua P[Mo''"; digunakan untuk deteksi fosfor secara spektroskopi.[18] Rentang tingkat oksidasi molibdenum yang lebar tercermin dari ragam molibdenum klorida:[16]
Struktur MoCl2 adalah cluster Mo dan empat anion klorida yang mengkompensasi muatan.[16]
Seperti kromium dan beberapa logam transisi lainnya, molibdenum membentuk ikatan rangkap empat, seperti pada Mo. Senyawa ini dapat diubah menjadi Mo, yang juga memiliki ikatan rangkap empat.[16]
Tingkat oksidasi 0 dimungkinkan dengan ligan karbon monoksida, seperti pada molibdenum heksakarbonil, Mo(CO)6.[16]
Molibdenit—bijih utama asal molibdenum sekarang diekstraksi—sebelumnya dikenal sebagai molibdena. Molibdena dirancukan dan sering digunakan seolah-olah itu adalah grafit. Seperti grafit, molibdenit bisa digunakan untuk menghitamkan permukaan atau sebagai pelumas padat.[19] Bahkan saat molibdena dapat dibedakan dari grafit, masih dibingungkan dengan bijih timbal PbS (sekarang disebut galena); nama itu berasal dari bahasa Yunani kuno Μόλυβδος molybdos, yang berarti timbal.[6] (Kata Yunani itu sendiri telah diusulkan sebagai kata serapan dari bahasa Anatolia, Luvia, dan bahasa Lydia).[20]
Meskipun molibdenum (dilaporkan) sengaja dipadu dengan baja dalam satu pedang Jepang abad ke-14 (tahun pembuatan 1330), seni itu tidak pernah digunakan secara luas dan kemudian punah.[21][22] Di Barat pada tahun 1754, Bengt Andersson Qvist memeriksa sampel molibdenit dan menentukan bahwa itu tidak mengandung timbal dan karenanya bukan galena.[23]
Pada tahun 1778 kimiawan Swedia, Carl Wilhelm Scheele, menyatakan dengan tegas bahwa molibdena (memang) bukan galena maupum grafit.[24][25] Sebagai gantinya, Scheele dengan tepat mengusulkan bahwa molibdena adalah bijih dari unsur baru yang berbeda, diberi nama molibdenum untuk mineral yang ada di dalamnya, dan dari situ bisa diisolasi. Peter Jacob Hjelm berhasil mengisolasi molibdenum dengan menggunakan karbon dan minyak biji rami pada tahun 1781.[6][26]
Pada abad berikutnya, molibdenum tidak mempunyai manfaat industrial. Ia relatif langka, logam murni sulit untuk diekstraksi, dan teknik metalurgi yang diperlukan belum matang.[27][28][29] Paduan baja molibdenum awal menunjukkan harapan besar untuk meningkatkan kekerasan, namun upaya pembuatan paduan dalam skala besar terhambat dengan hasil yang tidak konsisten, kecenderungan terhadap kerapuhan, dan rekristalisasi. Pada tahun 1906, William D. Coolidge mengajukan paten untuk menyediakan molibdenum ulet, yang mengarah pada aplikasi sebagai elemen pemanas untuk tungku suhu tinggi dan sebagai pendukung bola lampu filamen wolfram; pembentukan oksida dan degradasi mensyaratkan agar molibdenum disimpan rapat secara fisik atau disimpan dalam gas inert.[30] Pada tahun 1913, Frank E. Elmore mengembangkan proses flotasi buih untuk memulihkan molibdenit dari bijih; flotasi tetap merupakan proses isolasi utama.[31]
Selama Perang Dunia I, permintaan molibdenum meningkat tajam; ia digunakan baik dalam lapis baja dan sebagai pengganti wolfram pada baja kecepatan tinggi. Beberapa tank Inggris dilindungi oleh lapisan baja mangan setebal 75 mm (3,0 in), namun ini terbukti tidak efektif. Pelat baja mangan diganti dengan pelat baja molibdenum setebal 25 mm ([convert: unit tak dikenal]) yang jauh lebih ringan yang memungkinkan kecepatan lebih tinggi, manuver yang lebih lincah, dan perlindungan yang lebih baik.[6] Jerman juga menggunakan baja berdoping molibdenum untuk artileri berat, seperti dalam howitzer super berat Big Bertha,[32] karena baja tradisional meleleh pada suhu yang dihasilkan oleh propelan satu ton selongsong.[33] Setelah perang, permintaan menurun drastis sampai kemajuan metalurgi memungkinkan pengembangan ekstensif untuk aplikasi di masa damai. Pada Perang Dunia II, molibdenum kembali melihat kepentingan strategis sebagai pengganti wolfram dalam paduan baja.[34]

Molibdenum adalah unsur paling melimpah ke-54 dalam kerak bumi dan unsur paling melimpah ke-25 di samudera, dengan rata-rata 10 bagian per miliar; ini adalah unsur paling melimpah ke-42 di alam semesta.[6][35] Misi Rusia Luna 24 menemukan butir bantalan molibdenum (1 × 0,6 μm) dalam fragmen piroksena yang diambil dari Mare Crisium di permukaan bulan.[36] Kelangkaan molibdenum di kerak bumi diimbangi oleh konsentrasinya dalam sejumlah bijih yang tidak larut dalam air yang sering ditemukan. Ia sering tergabung dengan belerang dengan cara yang sama seperti tembaga. Meskipun molibdenum ditemukan di mineral seperti wulfenit (PbMoO4) dan powellit (CaMoO4), sumber komersial utamanya adalah molibdenit (MoS2). Molibdenum ditambang sebagai bijih utama dan juga dipulihkan sebagai produk sampingan dari pertambangan tembaga dan wolfram.[5]
Produksi molibdenum dunia adalah 250.000 t pada tahun 2011, produsen terbesar adalah China (94.000 t), Amerika Serikat (64.000 t), Chile (38.000 t), Peru (18.000 t) dan Meksiko (12.000 t). Total cadangan diperkirakan mencapai 10 juta ton, dan sebagian besar terkonsentrasi di China (4,3 Mt), AS (2,7 Mt) dan Chile (1,2 Mt). Berdasarkan benua, 93% produksi molibdenum dunia terbagi secara merata antara Amerika Utara, Amerika Selatan (terutama di Cile), dan China. Eropa dan seluruh Asia (kebanyakan Armenia, Rusia, Iran dan Mongolia) menghasilkan sisanya.[37]
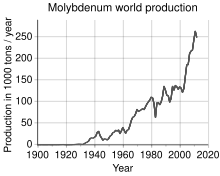
Dalam pengolahan molibdenit, bijih tersebut pertama kali dipanggang di udara pada suhu 700 °C (1.292 °F). Prosesnya menghasilkan gas belerang dioksida dan molibdenum(VI) oksida:[16]
Bijih yang teroksidasi biasanya diekstraksi dengan larutan amonia dalam air untuk menghasilkan amonium molibdat:
Tembaga, ketakmurnian dalam molibdenit, kurang larut dalam amonia. Untuk menghilangkannya dari larutan, tembaga diendapkan dengan hidrogen sulfida.[16] Amonium molibdat diubah menjadi amonium dimolibdat, yang diisolasi sebagai padatan. Memanaskan padatan ini menghasilkan molibdenum trioksida:[38]
Trioksida mentah dapat dimurnikan lebih lanjut dengan sublimasi pada 1.100 °C (2.010 °F).
Logam molibdenum dihasilkan melalui reduksi oksida dengan hidrogen:
Molibdenum untuk produksi baja direduksi melalui reaksi aluminotermal dengan penambahan besi untuk menghasilkan feromolibdenum. Bentuk umum feromolibdenum mengandung molibdenum 60%.[16][39]
Molibdenum memiliki nilai sekitar $30.000 per ton per Agustus 2009. Harga ini bertahan pada atau mendekati $10.000 per ton dari tahun 1997 sampai 2003, dan mencapai puncaknya $103.000 per ton pada bulan Juni 2005.[40] Pada tahun 2008 London Metal Exchange mengumumkan bahwa molibdenum akan diperdagangkan sebagai komoditas di bursa.[41]
Secara historis, tambang Knaben di selatan Norwegia, dibuka pada tahun 1885, merupakan tambang pertama yang didedikasikan untuk molibdenum. Tambang itu ditutup dari tahun 1973 sampai 2007, namun dibuka kembali tahun itu[42] dan sekarang menghasilkan 100.000 kilogram (98,42 ton panjang; 110,23 ton pendek) molibdenum disulfida per tahun. Tambang besar di Colorado (seperti tambang Henderson dan tambang Climax)[43] dan di British Columbia menghasilkan molibdenit sebagai produk utama mereka, sementara banyak deposit tembaga porfiri seperti Tambang Canyon Bingham di Utah dan tambang Chuquicamata di utara Chile menghasilkan molibdenum sebagai produk sampingan dari pertambangan tembaga.

Sekitar 86% molibdenum yang dihasilkan digunakan dalam bidang metalurgi, dan sisanya digunakan dalam aplikasi kimia. Perkiraan penggunaan global adalah baja struktural 35%, baja nirkarat 25%, bahan kimia 14%, alat & baja berkecepatan tinggi 9%, besi cor 6%, logam unsur molibdenum 6%, dan superalloy 5%.[44]
Molibdenum dapat menahan suhu ekstrim tanpa memuai atau melunak secara signifikan, membuatnya berguna di lingkungan yang panas, termasuk lapis baja militer, bagian pesawat terbang, stop kontak listrik, motor industri, dan filamen.[6][45]
Sebagian besar paduan baja berkecepatan tinggi (misalnya, baja 41xx mengandung 0,25% sampai 8% molibdenum.[5] Bahkan dalam porsi kecil ini, lebih dari 43.000 ton molibdenum digunakan setiap tahun dalam baja nirkarat, perkakas baja, besi cor, dan superalloy suhu tinggi.[35]
Molibdenum juga dinilai sebagai baja paduan untuk ketahanan korosi yang tinggi dan weldabilitas.[35][37] Molibdenum menyumbang ketahanan terhadap korosi pada baja nirkarat tipe-300 (khususnya tipe-316) dan terutama pada baja tahan karat super austenitik (seperti paduan AL-6XN, 254SMO atau 1925hMo). Molibdenum meningkatkan ketegangan kisi, sehingga meningkatkan energi yang dibutuhkan untuk melarutkan atom besi dari permukaan. Molibdenum juga digunakan untuk meningkatkan ketahanan korosi pada baja tahan karat feritik (misalnya kelas 444) dan baja tahan karat martensitik (misalnya 1.4122 dan 1.4418).
Molibdenum kadang digunakan sebagai pengganti wolfram karena kerapatannya yang lebih rendah dan harga yang lebih stabil.[35] Contohnya adalah baja berkecepatan tinggi seri 'M' seperti M2, M4 dan M42 sebagai substitusi untuk seri baja 'T', yang mengandung wolfram. Molibdenum dapat juga digunakan sebagai penyalut tahan api untuk logam lain. Meskipun titik lelehnya adalah 2.623 °C (4.753 °F), molibdenum cepat teroksidasi pada suhu di atas 760 °C (1.400 °F) membuatnya cocok untuk penggunaan dalam lingkungan vakum.[45]
TZM (Mo (~99%), Ti (~0.5%), Zr (~0.08%) dan sedikit C) adalah superalloy molibdenum tahan korosi yang tahan lelehan garam fluorida pada suhu di atas 1.300 °C (2.370 °F). Ia memiliki kekuatan sekitar dua kali kekuatan Mo murni, dan lebih ulet serta lebih mudah dilas. Selain itu, ia diuji menahan korosi garam eutaktik standar (FLiBe) dan uap garam yang digunakan dalam reaktor leburan garam selama 1100 jam dengan sangat sedikit korosi yang susah diukur.[46][47]
Logam paduan berbasis molibdenum lainnya yang tidak mengandung besi hanya memiliki aplikasi terbatas. Misalnya, baik molibdenum murni maupuan paduan molibdenum/wolfram (70%/30%) digunakan untuk pipa dan pompa pendesak yang kontak langsung dengan leburan zink, karena ketahanannya terhadap lelehan seng.[48]
Peran paling penting molibdenum dalam organisme hidup adalah sebagai logam heteroatom di tempat aktif dalam enzim tertentu.[64][65] Dalam fiksasi nitrogen bakterial, enzim nitrogenase yang terlibat dalam tahap terminal untuk mengurangi nitrogen molekuler biasanya mengandung molibdenum di tempat yang aktif (meskipun penggantian molibdenum dengan besi atau vanadium juga diketahui). Struktur pusat katalitik enzim serupa seperti yang terdapat dalam protein besi-belerang: ia menggabungkan Fe dan beberapa cluster MoFe.[66]
Reaksi yang dilakukan enzim nitrogenase adalah:
Dengan proton dan elektron dari rantai transportasi elektron, nitrogen direduksi menjadi amonia dan gas hidrogen bebas. Proses ini menggunakan energi, memerlukan pemecahan (hidrolisis) ATP menjadi ADP ditambah fosfat bebas (Pi).
Pada tahun 2008, dilaporkan bukti-bukti bahwa kelangkaan molibdenum di awal lautan di bumi merupakan faktor pembatas selama hampir dua miliar tahun dalam evolusi lebih lanjut dari kehidupan eukariotik (yang mencakup semua tumbuhan dan hewan). Rantai penyebabnya adalah sebagai berikut:[67]
Namun, sekali oksigen terbentuk di air loaut oleh eukariota yang terbatas tersebut, ia bereaksi dengan ir dan molibdenum dalam mineral di dasar laut menghasilkan molibdat yang dapat larut, membuatnya tersedia untuk bakteri fiksasi nitrogen. Bakteri-bakteri tersebut menyediakan senyawa Nitrogen produk fiksasi yang dapat digunakan oleh kehidupan yang lebih tinggi.
Meskipun oksigen di satu sisi mempromosikan fiksasi nitrogen dengan membuat molibdenum yang tersedia dalam air, ia juga secara langsung meracuni enzim nitrogenase. Jadi, dalam sejarah purba Bumi, setelah oksigen tiba dalam jumlah besar di udara dan air di Bumi, organisme yang terus memperbaiki nitrogen dalam kondisi aerobik terisolasi dan melindungi enzim penguat nitrogen mereka dari terlalu banyak oksigen dalam struktur heterosista atau yang setara. Isolasi struktural reaksi fiksasi nitrogen pada organisme aerobik terus berlanjut hingga saat ini.

Meskipun molibdenum membentuk senyawa dengan berbagai molekul organik, termasuk karbohidrat dan asam amino, ia ditransportasikan ke seluruyh tubuh manusia sebagai MoO.[71] Sekurang-kurangnya 50 enzim yang mengandung molibdenum diketahui pada tahun 2002, sebagian besar dalam bakteria, dan jumlahnya terus meningkat setiap tahun;[72][73] enzim tersebut termasuk aldehida oksidase, sulfit oksidase dan xantin oksidase.[6] Pada beberapa hewan, dan pada manusia, oksidasi xantin menjadi asam urat, suatu proses katabolisme purin, dikatalisis oleh xantin oksidase, suatu enzim yang mengandung molibdenum. Aktivitas xantin oksidase berbanding langsung dengan jumlah molibdenum dalam tubuh. Namun, konsentrasi molibdenum yang sangat tinggi dapat membalikkan tren dan dapat bertindak sebagai inhibitor baik untuk katabolisme purin maupun proses-proses lainnya. Konsentrasi molibdenum juga berpengaruh pada sintesis protein, metabolisme, dan pertumbuhan.[71]
Pada hewan dan tumbuhan, senyawa trisiklik yang disebut molibdopterin (yang, terlepas dari namanya, tidak mengandung molibdenum) bereaksi dengan molibdat membentuk kofaktor lengkap yang mengandung molibdenum yang disebut kofaktor molibdenum. Selain nitrogenase kuno secara filogenetika (seperti yang didiskusikan di atas) bahwa fiksasi nitrogen terjadi di dalam beberapa bakteri dan sianobakteri, seluruh enzim yang menggunakan molibdenum (sejauh yang sudah diidentifikasi) menggunakan kofaktor molibdenum, di mana molibdenum berada pada tingkat oksidasi VI, sama seperti molibdat.[74] Enzim molibdenum pada tumbuhan dan hewan mengkatalisis oksidasi dan kadang-kadang reduksi beberapa molekul kecil dalam proses yang mengatur siklus nitrogen, belerang, dan karbon.[75]
Molibdenum adalah unsur makanan renik yang diperlukan untuk kelangsungan hidup manusia dan beberapa mamalia yang telah dipelajari.[76] Diketahui empat enzim Mo-dependen mamalia, semuanya mengandung kofaktor molibdenum (Moco) berbasis pterin di situs aktif mereka: sulfit oksidase, xantin oksidoreduktase, aldehida oksidase, dan amidoksime reduktase mitokondrial.[77] Orang yang sangat kekurangan molibdenum memiliki sulfit oksidase buruk fungsi dan rentan terhadap reaksi toksik terhadap sulfit dalam makanan.[78][79] Tubuh manusia mengandung sekitar 0,07 mg molibdenum per kilogram berat badan,[80] dengan konsentrasi yang lebih tinggi terdapat pada liver dan ginjal dan lebih rendah pada tulang belakang.[35] Molybdenum juga hadir dalam enamel gigi manusia dan dapat membantu mencegah pembusukannya.[81]
Rata-rata asupan harian molibdenum bervariasi antara 0,12 dan 0,24 mg, tergantung pada kandungan molibdenum makanan.[82] Daging babi, domba, dan daging sapi masing-masing memiliki sekitar 1,5 bagian per juta molibdenum. Sumber makanan penting lainnya termasuk kacang hijau, telur, biji bunga matahari, tepung terigu, lentil, mentimun dan biji sereal.[6] Toksisitas akut belum terlihat pada manusia, dan toksisitasnya sangat bergantung pada keadaan kimia. Studi pada tikus menunjukkan median dosis letal (LD50) serendah 180 mg/kg untuk beberapa senyawa Mo.[83] Meskipun data toksisitas manusia tidak tersedia, penelitian pada hewan menunjukkan bahwa konsumsi kronis lebih dari 10 mg/hari molibdenum dapat menyebabkan diare, retardasi pertumbuhan, infertilitas, berat lahir rendah, dan encok; ini juga dapat mempengaruhi paru-paru, ginjal, dan liver.[82][84] Natrium wolframat adalah inhibitor kompetitif molibdenum. Wolfram diet mengurangi konsentrasi molibdenum dalam jaringan.[35]
Konsentrasi tanah molibdenum yang rendah dalam kelompok geografis dari utara Cina hingga Iran menyebabkan defisiensi molibdenum, dan dikaitkan dengan peningkatan kanker esofagus.[85][86] Dibandingkan dengan Amerika Serikat, yang memiliki pasokan molibdenum lebih besar di dalam tanah, orang-orang yang tinggal di daerah tersebut memiliki risiko sekitar 16 kali lebih besar untuk karsinoma sel skuamosa esofagus.[87]
Defisiensi molibdenum juga telah dilaporkan sebagai konsekuensi pemberian nutrisi parenteral total non-molibdenum (pemberian makanan intravena lengkap) dalam jangka waktu yang lama. Ini menghasilkan tingkat sulfit dan urat darah yang tinggi, sama seperti defisiensi kofaktor molibdenum. Namun (mungkin karena penyebab defisiensi molibdenum murni ini terjadi terutama pada orang dewasa), konsekuensi neurologisnya tidak begitu mengemuka seperti pada kasus defisiensi kofaktor bawaan.[88]
Penyakit defisiensi kofaktor molibdenum bawaan, yang terlihat pada bayi, adalah ketidakmampuan untuk mensintesis kofaktor molibdenum, sebuah molekul heterosiklik yang mengikat molibdenum di tempat aktif di semua enzim manusia yang diketahui menggunakan molibdenum. Defisiensi yang dihasilkan menghasilkan tingkat sulfit dan urat yang tinggi, dan kerusakan neurologis.[89][90]
Kandungan molibdenum tinggi dalam tubuh dapat mengganggu asupan tembaga yang mengakibatkan defisiensi tembaga. Molibdenum mencegah protein plasma mengikat tembaga, dan juga meningkatkan jumlah tembaga yang diekskresikan dalam air seni. Pemamah biak (ruminant) yang mengkonsumsi kadar molibdenum tinggi menderita diare, pertumbuhan kerdil, anemia, dan akromotrikia (hilangnya pigmen bulu). Gejala ini dapat diatasi dengan suplemen tembaga, baik melalui diet maupun injeksi.[91] Kekurangan tembaga efektif, dapat diperparah dengan kelebihan belerang.[35][92]
Defisiensi tembaga dapat pula sengaja diinduksi untuk tujuan pengobatan, dengan menggunakan senyawa amonium tetratiomolibdat. Anion tetratiomolibdat yang berwarna merah cerah merupakan zat pengkhelat tembaga. Tetratiomolibdat pertama kali digunakan dalam terapi untuk pengobatan toksikosis tembaga pada hewan. Ia kemudian dikenalkan sebagai perawatan dalam penyakit Wilson, suatu kelainan herediter terkait metabolisme tembaga pada manusia. Ia bertindak dengan menyaingi absorpsi tembaga dalam usus dan meningkatkan ekskresi. Telah ditemukan pula bahwa tetratiomolibdat memiliki efek inhibisi pada angiogenesis, yang secara potensial menghambat proses translokasi membran yang bergantung pada ion tembaga..[93] Ini adalah hal yang menjanjikan dalam penelitian pengobatan kanker, degenerasi makular terkait usia, dan penyakit lain yang melibatkan proliferasi patologis pembuluh darah.[94][95]
Debu dan uap molibdenum, dihasilkan dari penambangan atau karya logam, bersifat toksik, terutama jika terhirup (termasuk debu yang terjebak dalam sinus pranasal dan kemudian tertelan).[83] Paparan jangka panjang dengan tingkat rendah dapat menyebabkan iritasi pada mata dan kulit. Harus dihindari untuk menelan atau menghirup langsung molibdenum dan oksidanya.[96][97] Peraturan OSHA menetapkan paparan molibdenum maksimum yang diizinkan dalam 8-jam per hari sebagai 5 mg/m3. Paparan kronis mulai 60 hingga 600 mg/m3 dapat menyebabkan gejalan termsuk kelelahan, sakit kepala dan ngilu sendi.[98] Pada level 5000 mg/m3, molibdenum membahayakan segera terhadap kesehatan dan kehidupan (IDLH).[99]
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||