Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
Un enol es un alqueno que posee un grupo hidroxilo unido a uno de los átomos de carbonos del doble enlace. A este grupo funcional se lo denomina grupo enol; aunque es más común utilizar el término enol para referirse a los alquenoles, que el término alquenol mismo. Los enoles y los grupos carbonilo (como las cetonas y los aldehídos) son, de hecho, isómeros; esto es lo que se llama tautomería ceto-enol:
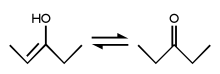
La forma enol es la mostrada en la izquierda. Usualmente es inestable, no sobrevive mucho, y cambia a la forma ceto (al isómero cetona), dibujada a la derecha. Esto se debe a que el oxígeno es más electronegativo que el carbono, y por eso tiene más fuerza su enlace. Un doble enlace carbono=oxígeno es más de dos veces más fuerte que un enlace carbono-oxígeno simple, pero un enlace carbono-carbono doble no es el doble de fuerte que dos enlaces simples carbono-carbono sino algo menos.
Solo en los compuestos 1,2-dicarbonilos y 1,3,5-tricarbonilos predomina la forma (mono)enol. En este caso es por una resonancia y por un puente hidrógeno intramolecular que tiene la forma enol, pero que no puede tener la forma ceto. Entonces, el propanodial (O=CH-CH2-CH=O) existe más de un 99% como un monoenol.
La palabra enol deriva de alqueno (o simplemente -eno, su sufijo) y alcohol (o el sufijo -ol).
Cuando un enol pierde el Hα (el Hα es el H del Cα, y este es el que es vecino del C carbonilo), se forma el anión enolato como se muestra a continuación:
Los 1,3 dicarbonilos y 1,3,5 tricarbonilos son levemente ácidos, por la fuerte estabilidad de resonancia. Estos aniones enolato son muy preciados a la hora de sintetizar alcoholes y compuestos carbonilos muy complejos, como Enol (Adición aldólica). El valor sintético está dado gracias a que es nucleofílico, por tener una carga negativa neta.
Cuando el carbonilo de una aciloína con un hidrógeno α disponible presenta tautomería ceto-enol, se interconvierte a un enodiol. Este compuesto puede formar un segunda aciloína regioisomérica:

En química de carbohidratos, la tautomería de los carbonilos con un hidroxilo α se denomina transposición de Lobry de Bruyn–van Ekenstein, en donde la tautomería es catalizada por ácidos o bases y se interconvierte una aldosa a cetosa, formándose un enodiol como intermediario. Sucesivamente, las cetosas pueden ser transformadas a 3-cetosas, etcétera. El enodiol también es un intermediario para la epimerización de una aldosa o cetosa.[1][2]
Los enodioles son reductores, y al estar conjugados con un carbonilo se define el grupo funcional reductona. Estos compuestos son donadores de electrones eficientes y el ejemplo biológico clásico es el ácido ascórbico.