Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.

El ácido ribonucleico o ARN es un ácido nucleico que participa en procesos biológicos esenciales para los seres vivos junto con el ADN y las proteínas. Está presente tanto en las células procariotas como en las eucariotas, y es el único material genético de ciertos virus (los virus ARN).
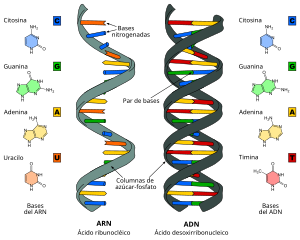
Desde el punto de vista químico, el ARN es un polinucleótido formado por una cadena simple de ribonucleótidos.[1][2] Cada uno de estos se compone de una ribosa, un fosfato y una de las cuatro bases nitrogenadas (adenina, guanina, citosina y uracilo).[3] El ARN celular es lineal y monocatenario (de una sola cadena), pero en el genoma de algunos virus es de doble hebra.[4]
La principal función biológica en la que participa el ARN es dirigir las etapas intermedias de la síntesis proteica. El ADN contiene la información para la síntesis de las proteínas necesarias para el desarrollo y funcionamiento de la célula. Esta información es transferida al ARN mensajero (ARNm) en la transcripción del ADN; posteriormente se produce la traducción del ARNm, donde el ARN transferente (ARNt) envía aminoácidos hasta el ARN ribosómico (ARNr), el cual enlaza los aminoácidos y construye las proteínas.[5] El ARN también participa en otras funciones esenciales como la regulación de la expresión génica (ej.: ARN largo no codificante (ARNlnc) o el ARN pequeño de interferencia (ARNpi)) y la modificación post-transcripcional del ARNm (ej.: ARN pequeño nuclear).
Los ácidos nucleicos fueron descubiertos en 1867 por Friedrich Miescher, que los llamó nucleína, ya que los aisló del núcleo celular.[6] Más tarde, se comprobó que las células procariotas, que carecen de núcleo, también contenían ácidos nucleicos. El papel del ARN en la síntesis de proteínas fue sospechado en 1939.[7] Severo Ochoa ganó el Premio Nobel de Medicina en 1959 tras descubrir cómo se sintetizaba el ARN.[8]
En 1965 Robert W. Holley halló la secuencia de 77 nucleótidos de un ARN de transferencia de una levadura,[9] con lo que obtuvo el Premio Nobel de Medicina en 1968. En 1967, Carl Woese comprobó las propiedades catalíticas de algunos ARN y sugirió que las primeras formas de vida usaron ARN como portador de la información genética tanto como catalizador de sus reacciones metabólicas (hipótesis del mundo de ARN).[10][11] En 1976, Walter Fiers y sus colaboradores determinaron la secuencia completa del ARN del genoma de un virus ARN (bacteriófago MS2).[12]
En 1990 se descubrió en la Petunia que genes introducidos pueden silenciar genes similares de la misma planta, lo que condujo al descubrimiento del ARN interferente.[13][14] Aproximadamente al mismo tiempo se hallaron los micro-ARN, pequeñas moléculas de 22 nucleótidos que tenían algún papel en el desarrollo de Caenorhabditis elegans.[15] El descubrimiento de ARN que regulan la expresión génica ha permitido el desarrollo de medicamentos hechos de ARN, como los ARN pequeños de interferencia que silencian genes.[16]
En el año 2023 se tiene comprobado que las moléculas de ARN fueron la primera forma de vida propiamente dicha en habitar el planeta Tierra (Hipótesis del mundo de ARN).

Como el ADN, el ARN está formado por una cadena de monómeros repetitivos llamados nucleótidos. Los nucleótidos se unen uno tras otro mediante enlaces fosfodiéster cargados negativamente.
Cada nucleótido está formado por tres componentes:
| ARN | ADN | |
|---|---|---|
| Pentosa | Ribosa | Desoxirribosa |
| Purinas | Adenina y Guanina | Adenina y Guanina |
| Pirimidinas | Citosina y Uracilo | Citosina y Timina |
Los carbonos de la ribosa se numeran de 1' a 5' en sentido horario. La base nitrogenada se une al carbono 1'; el grupo fosfato se une al carbono 5' y al carbono 3' de la ribosa del siguiente nucleótido. El pico tiene una carga negativa a pH fisiológico lo que confiere al ARN carácter polianiónico. Las bases púricas (adenina y guanina) pueden formar puentes de hidrógeno con las pirimidínicas (uracilo y citosina) según el esquema C=G y A=U.[17] Además, son posibles otras interacciones, como el apilamiento de bases[18] o tetrabucles con apareamientos G=A.[17] Muchos ARN contienen además de los nucleótidos habituales, nucleótidos modificados, que se originan por transformación de los nucleótidos típicos; son característicos de los ARN de transferencia (ARNt) y el ARN ribosómico (ARNr); también se encuentran nucleótidos metilados en el ARN mensajero eucariótico.[19]

La interacción por puentes de hidrógeno descrita por Watson y Crick[20] forma pares de bases entre una purina y una pirimidina. A este patrón se le conoce como apareamiento Watson y Crick. En este, la adenina se aparea con el uracilo (timina, en ADN) y la citosina con la guanina. Sin embargo, en el ARN se presentan muchas otras formas de apareamiento, de las cuales la más ubicua es el apareamiento wobble (también apareamiento por balanceo o apareamiento titubeante) para la pareja G-U. Este fue propuesto por primera vez por Crick para explicar el apareamiento codón-anticodón en los ARNt y ha sido confirmado en casi todas las clases de ARN en los tres dominios filogenéticos.[21]
Se refiere a la secuencia lineal de nucleótidos en la molécula de ARN. Los siguientes niveles estructurales (estructura secundaria, terciaria) son consecuencia de la estructura primaria. Además, la secuencia misma puede ser información funcional; esta puede traducirse para sintetizar proteínas (en el caso del ARNm) o funcionar como región de reconocimiento, región catalítica, entre otras.
Estructura primaria de tRNAPhe

El ARN se pliega como resultado de la presencia de regiones cortas con apareamiento intramolecular de bases, es decir, pares de bases formados por secuencias complementarias más o menos distantes dentro de la misma hebra. La estructura secundaria se refiere, entonces, a las relaciones de apareamiento de bases: «El término ‘estructura secundaria’ denota cualquier patrón plano de contactos por apareamiento de bases. Es un concepto topológico y no debe ser confundido con algún tipo de estructura bidimensional».[22] La estructura secundaria puede ser descrita a partir de motivos estructurales que se suelen clasificar de la siguiente manera:
| Hélice
(tallo, stack) |
Región con bases apareadas. | |
|---|---|---|
| Bucle
(ciclo, loop) |
Región incluida en una hélice en donde las bases no están apareadas. | 
|
| Bucle en horquilla
(tallo y bucle, hairpin loop) |
Estructura en donde regiones cercanas de bases complementarias se aparean, separadas por una región no apareada que permite que la secuencia se doble para formar una hélice. | 
|
| Bucle interno
(internal loop) |
Estructura en donde hay regiones no apareadas en ambos lados de la hebra. Puede ser simétrico o asimétrico. | 
|
| Protuberancia
(buldge) |
Estructura en donde hay una región no apareada en un solo lado de la hebra. |  |
| Bucle múltiple
(helical junction) |
Región en donde se juntan múltiples hélices. | 
|
| Pseudonudo | Variación de bucle en donde solo una parte del bucle sí está apareada. El pseudonudo más simple consiste de una región libre del ARN apareada con un bucle. | 
|

La estructura terciaria es el resultado de las interacciones en el espacio entre los átomos que conforman la molécula. Algunas interacciones de este tipo incluyen el apilamiento de bases y los apareamientos de bases distintos a los propuestos por Watson y Crick, como el apareamiento Hoogsteen, los apareamientos triples y los zíperes de ribosa.

A diferencia del ADN las moléculas de ARN suelen ser de cadena simple y no forman hélices dobles extensas, no obstante, en las regiones con bases apareadas sí forma hélices como motivo estructural terciario. Una importante característica estructural del ARN que lo distingue del ADN es la presencia de un grupo hidroxil en posición 2' de la ribosa, que causa que las dobles hélices de ARN adopten una conformación A, en vez de la conformación B que es la más común en el ADN.[24] Esta hélice A tiene un surco mayor muy profundo y estrecho y un surco menor amplio y superficial.[25] Una segunda consecuencia de la presencia de dicho hidroxilo es que los enlaces fosfodiéster del ARN de las regiones en que no se forma hélice doble son más susceptibles de hidrólisis química que los del ADN; los enlaces fosfodiéster del ARN se hidrolizan rápidamente en disolución alcalina, mientras que los enlaces del ADN son estables.[26] La vida media de las moléculas de ARN es mucho más corta que las del ADN, de unos minutos en algunos ARN bacterianos o de unos días en los ARNt humanos.[19]
La biosíntesis de ARN está catalizada normalmente por la enzima ARN polimerasa que usa una hebra de ADN como molde, proceso conocido con el nombre de transcripción. Por tanto, todos los ARN celulares provienen de copias de genes presentes en el ADN.
La transcripción comienza con el reconocimiento por parte de la enzima de un promotor, una secuencia característica de nucleótidos en el ADN situada antes del segmento que va a transcribirse; la hélice doble del ADN es abierta por la actividad helicasa de la propia enzima. A continuación, la ARN polimerasa progresa a lo largo de la hebra de ADN en sentido 3' → 5', sintetizando una molécula complementaria de ARN; este proceso se conoce como elongación, y el crecimiento de la molécula de ARN se produce en sentido 5' → 3'. La secuencia de nucleótidos del ADN determina también dónde acaba la síntesis del ARN, gracias a que posee secuencias características que la ARN polimerasa reconoce como señales de terminación.[27]
Tras la transcripción, la mayoría de los ARN son modificados por enzimas. Por ejemplo, al pre-ARN mensajero eucariota recién transcrito se le añade un nucleótido de guanina modificado (7-Metilguanosina) en el extremo 5' por medio de un puente de trifosfato formando un enlace 5'→ 5' único, también conocido como «capucha» o «caperuza», y una larga secuencia de nucleótidos de adenina en el extremo 3' (cola poli-A); posteriormente se le eliminan los intrones (segmentos no codificantes) en un proceso conocido como empalme o ayuste.
En virus, hay también varias ARN polimerasas ARN-dependientes que usan ARN como molde para la síntesis de nuevas moléculas de ARN. Por ejemplo, varios virus ARN, como los poliovirus, usan este tipo de enzimas para replicar su genoma.[28][29]
La principal función del ARN es dirigir la síntesis de proteinas, a partir de la información obtenida del ADN. Las clases de ARN, según la fase, son los siguientes:
El ARN mensajero (ARNm) es el tipo de ARN que lleva la información del ADN a los ribosomas, el lugar de la síntesis de proteínas. La secuencia de nucleótidos del ARNm determina la secuencia de aminoácidos de la proteína.[30] Por ello, el ARNm es denominado ARN codificante.
No obstante, muchos ARN no codifican proteínas, y reciben el nombre de ARN no codificantes; se originan a partir de genes propios (genes ARN), o son los intrones rechazados durante el proceso de empalme o ayuste. Son ARN no codificantes el ARN de transferencia (ARNt) y el ARN ribosómico (ARNr), que son elementos fundamentales en el proceso de traducción, y diversos tipos de ARN reguladores.[31]
Ciertos ARN no codificantes, denominados ribozimas, son capaces de catalizar reacciones químicas como cortar y unir otras moléculas de ARN,[32] o formar enlaces peptídicos entre aminoácidos en el ribosoma durante la síntesis de proteínas.[33]

El ARN mensajero (ARNm) es el que lleva la información sobre la secuencia de aminoácidos de la proteína desde el ADN, lugar en que está inscrita, hasta el ribosoma, lugar en que se sintetizan las proteínas de la célula. Es por lo tanto, una molécula intermediaria entre el ADN y la proteína, y el apelativo de «mensajero», es del todo descriptivo. En los eucariotas, el ARNm se sintetiza en el nucleoplasma del núcleo celular y donde es procesado antes de acceder al citosol, donde se hallan los ribosomas, a través de los poros de la envoltura nuclear.
Los ARN de transferencia (ARNt) son cortos polímeros de unos 80 nucleótidos, que transfiere un aminoácido específico al polipéptido en crecimiento; se unen a lugares específicos del ribosoma durante la traducción. Tienen un sitio específico para la fijación del aminoácido (extremo 3') y un anticodón formado por un triplete de nucleótidos que se une al codón complementario del ARNm mediante puentes de hidrógeno.[31] Estos ARNt, al igual que otros tipos de ARN, pueden ser modificados post-transcripcionalmente por enzimas. La modificación de alguna de sus bases es crucial para la descodificación de ARNm y para mantener la estructura tridimensional del ARNt.[34]
El ARN ribosómico (ARNr) se halla combinado con proteínas para formar los ribosomas, donde representa unas 2/3 partes de los mismos. En procariotas, la subunidad mayor del ribosoma contiene dos moléculas de ARNr y la subunidad menor, una. En los eucariotas, la subunidad mayor contiene tres moléculas de ARNr y la menor, una. En ambos casos, sobre el armazón constituido por los ARNm se asocian proteínas específicas. El ARNr es muy abundante y representa el 80 % del ARN hallado en el citoplasma de las células eucariotas.[35] Los ARN ribosómicos son el componente catalítico de los ribosomas; se encargan de crear los enlaces peptídicos entre los aminoácidos del polipéptido en formación durante la síntesis de proteínas; actúan, pues, como ribozimas.
Muchos tipos de ARN regulan la expresión génica gracias a que son complementarios de regiones específicas del ARNm o de genes del ADN.
Los ARN interferentes (ARNi) son moléculas de ARN que suprimen la expresión de genes específicos mediante mecanismos conocidos globalmente como ribointerferencia o interferencia por ARN. Los ARN interferentes son moléculas pequeñas (de 20 a 25 nucléotidos) que se generan por fragmentación de precursores más largos. Se pueden clasificar en tres grandes grupos:[36]
Los micro-ARN (miARN) son cadenas cortas de 21 o 22 nucleótidos hallados en células eucariotas que se generan a partir de precursores específicos codificados en el genoma. Al transcribirse, se pliegan en horquillas intramoleculares y luego se unen a enzimas formando un complejo efector que puede bloquear la traducción del ARNm o acelerar su degradación comenzando por la eliminación enzimática de la cola poli A.[37][38]
Los ARN interferentes pequeños (ARNpi o siARN), formados por 20-25 nucleótidos, se producen con frecuencia por rotura de ARN víricos, pero pueden ser también de origen endógeno.[39][40] Tras la transcripción se ensambla en un complejo proteico denominado RISC (RNA-induced silencing complex) que identifica el ARNm complementario que es cortado en dos mitades que son degradadas por la maquinaria celular, bloquean así la expresión del gen.[41][42][43]
Los ARN asociados a Piwi[44] son cadenas de 29-30 nucleótidos, propias de animales; se generan a partir de precursores largos monocatenarios (formados por una sola cadena), en un proceso que es independiente de Drosha y Dicer. Estos ARN pequeños se asocian con una subfamilia de las proteínas "Argonauta" denominada proteínas Piwi. Son activos las células de la línea germinal; se cree que son un sistema defensivo contra los transposones y que juegan algún papel en la gametogénesis.[45][46]
Un ARN antisentido es la hebra complementaria (no codificadora) de un hebra ARNm (codificadora). La mayoría inhiben genes, pero unos pocos activan la transcripción.[47] El ARN antisentido se aparea con su ARNm complementario formando una molécula de hebra doble que no puede traducirse y es degradada enzimáticamente.[48] La introducción de un transgen codificante para un ARNm antisentido es una técnica usada para bloquear la expresión de un gen de interés. Un mARN antisentido marcado radioactivamente puede usarse para mostrar el nivel de transcripción de genes en varios tipos de células. Algunos tipos estructurales antisentidos son experimentales, ya que se usan como terapia antisentido.
Muchos ARN largos no codificantes (ARNnc largo) regulan la expresión génica en eucariotas;[49] uno de ellos es el Xist que recubre uno de los dos cromosomas X en las hembras de los mamíferos inactivándolo (corpúsculo de Barr).[50] Diversos estudios revelan que es activo a bajos niveles. En determinadas poblaciones celulares, una cuarta parte de los genes que codifican para proteínas y el 80 % de los lncRNA detectados en el genoma humano están presentes en una o ninguna copia por célula, ya que existe una restricción en determinados ARN.[51]
Un interruptor molecular o ribointerruptor es una parte del ARNm (ácido ribonucleico mensajero) al cual pueden unirse pequeñas moléculas que afectan la actividad del gen.[52][53][54] Por tanto, un ARNm que contenga un interruptor molecular está directamente implicado en la regulación de su propia actividad que depende de la presencia o ausencia de la molécula señalizadora. Tales ribointerruptores se hallan en la región no traducida 5' (5'-UTR), situada antes del codón de inicio (AUG), y/o en la región no traducida 3' (3'-UTR), también llamada secuencia de arrastre,[19] situada entre el codón de terminación (UAG, UAA o UGA) y la cola poli A.[54]

El ARN puede actuar como biocatalizador. Ciertos ARN se asocian a proteínas formando ribonucleoproteínas y se ha comprobado que es la subunidad de ARN la que lleva a cabo las reacciones catalíticas; estos ARN realizan las reacciones in vitro en ausencia de proteína. Se conocen cinco tipos de ribozimas; tres de ellos llevan a cabo reacciones de automodificación, como eliminación de intrones o autocorte, mientras que los otros (ribonucleasa P y ARN ribosómico) actúan sobre substratos distintos.[19] Así, la ribonucleasa P corta un ARN precursor en moléculas de ARNt,[55] mientras que el ARN ribosómico realiza el enlace peptídico durante la síntesis proteica ribosómica.
Los intrones son separados del pre-ARNm durante el proceso conocido como «ayuste» por los espliceosomas, que contienen numerosos ARN pequeños nucleares (ARNpn).[56] En otros casos, los propios intrones actúan como ribozimas y se separan a sí mismos de los exones.[57]
Los ARN pequeños nucleolares (ARNpno), hallados en el nucléolo y en los cuerpos de Cajal, dirigen la modificación de nucleótidos de otros ARN;[31] el proceso consiste en transformar alguna de las cuatro bases nitrogenadas típicas (A, C, U, G) en otras. Los ARNpno se asocian con enzimas y los guían apareándose con secuencias específicas del ARN al que modificarán. Los ARNr y los ARNt contienen muchos nucleótidos modificados.[58][59]
La mitocondrias tienen su propio aparato de síntesis proteica, que incluye ARNr (en los ribosomas), ARNt y ARNm. Los ARN mitocondriales (ARNmt o mtARN) representan el 4 % del ARN celular total. Son transcritos por una ARN polimerasa mitocondrial específica.[19]
El ADN es la molécula portadora de la información genética en todos los organismos celulares, pero, al igual que el ADN, el ARN puede guardar información genética. Los virus ARN carecen por completo de ADN y su genoma está formado por ARN, el cual codifica las proteínas del virus, como las de la cápside y algunos enzimas. Dichos enzimas realizan la replicación del genoma vírico. Los «viroides» son otro tipo de patógenos que consisten exclusivamente en una molécula de ARN que no codifica ninguna proteína y que es replicado por la maquinaria de la célula hospedadora.[60]
La hipótesis del mundo de ARN propone que el ARN fue el primer ácido nucleico que apareció en la Tierra precediendo posteriormente al ADN y a su vez estos ácidos nucleicos junto con proteínas al unirse con liposomas formados espontáneamente originarían las primeras células. Se basa en la comprobación de que el ARN puede contener información genética, de un modo análogo a como lo hace el ADN, y que algunos tipos son capaces de llevar a cabo reacciones metabólicas, como autocorte o formación de enlaces peptídicos.
Durante años se especuló en qué fue primero, el ADN o las enzimas, ya que las enzimas se sintetizan a partir del ADN y la síntesis de ADN es llevada a cabo por enzimas. Si se supone que las primeras formas de vida usaron el ARN tanto para almacenar su información genética como realizar su metabolismo, se supera este escollo. Experimentos con los ribozimas básicos, como el ARN viral Q-beta, han demostrado que las estructuras de ARN autorreplicantes sencillas pueden resistir incluso a fuertes presiones selectivas (como los terminadores de cadena de quiralidad opuesta).[61]
|página= y |páginas= redundantes (ayuda). PMID 15138502. doi:10.1371/journal.pbio.0020133.