Type a search term to find related articles by LIMS subject matter experts gathered from the most trusted and dynamic collaboration tools in the laboratory informatics industry.
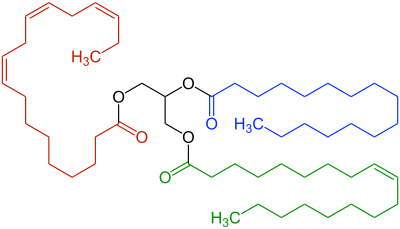


Lipolyse (englisch lipolysis, von altgriechisch λίπος lípos, deutsch ‚Fett‘ und λύσις lýsis, deutsch ‚Auflösung‘) ist die hydrolytische Spaltung verseifbarer Lipide, d. h. von Triglyceriden (Fetten) und Cholesterinestern durch Enzyme aus der Gruppe der Lipasen. Beim Abbau entstehen – neben Mono- und Diglyceriden als Zwischenprodukten – freie Fettsäuren, die ins Blut abgegeben werden, sowie einer der Alkohole Glycerin oder Cholesterin. Die Lipolyse tritt bei tierischen Organismen vorwiegend bei der Mobilisierung von Depotfett aus den Adipozyten des Fettgewebes,[1] im geringen Umfang auch bei der Fettverdauung auf, wobei das Enzym Pankreaslipase eingesetzt wird. Die gebildeten Fettsäuren werden über die sogenannte β-Oxidation unter Energiegewinnung weiter zerlegt. Der Prozess der Lipolyse ist umkehrbar; Organismen können in der Lipogenese aus Kohlenhydraten wie Glucose Fettsäuren und daraus Fette synthetisieren.
Etwa 15 % der Esterbindungen aufgenommener Triacylglyceride werden im Magen gespalten, der Hauptteil im Darm, wobei aber hauptsächlich Monoacylglyceride und Fettsäuren entstehen. Die verbleibenden Monoester lagern sich mit längerkettigen Fettsäuren zu Micellen zusammen, welche passiv durch die Zellmembranen in die Darmschleimhaut (Mukosa) diffundieren. Hier werden die Fettsäuren, Mono- und Diacylglyceride wieder zu Fetten umgewandelt und zusammen mit Cholesterin und Cholesterinester, Phospholipiden und Lipoproteinen zu den Chylomikronen zusammengelagert. Diese stellen die eigentliche Transportform für Lipide dar; hiermit werden die aus der Nahrung aufgenommenen Lipide hauptsächlich in die Fettzellen, die sogenannten Adipozyten, teils auch in Leber und Muskelgewebe transportiert. Die eigentliche Lipolyse läuft vorwiegend in den Fettzellen ab. Fette sind die bedeutendste Energiereserve des Menschen.[2] Fast alle Tiere verwenden Lipide als längerfristige Speicherform und in fast allen Tieren in Form von Triglyceriden, nur einige Fische speichern Energie längerfristig in Wachsen,[3] beispielsweise beim Escolar. Die meisten Tiere haben für die Speicherung von Fetten spezialisierte Zellen (Adipozyten), während einige Fische ihre Energie in Muskelgeweben oder in der Leber speichern.[3]
Im Magen spalten die Magenlipasen Fette zu Mono- und Diglyceriden. Obwohl diese Lipasen ein pH-Optimum von 5–7 haben, arbeiten sie auch im stark sauren Bereich im Magen sehr effektiv; der Anteil an der gesamten Esterspaltung ist jedoch mit etwa 15 % gering.[4]
Im Dünndarm spaltet die Pankreaslipase die Fette hauptsächlich zu β-Monoglyceriden. Carboxylesterasen und Gallensalz-aktivierte Lipasen spalten neben Fetten auch Cholesterinester und β-Monoglyceride vollständig zu Fettsäuren und dem jeweiligen Alkohol.
Das Fettgewebe dient als körpereigenes Fettdepot zur Energielieferung.[5] Hier werden bei Bedarf über eine lipolytische Kaskade Triglyceride zu Glycerin und Fettsäuren abgebaut.[6] Das geschwindigkeitsbestimmende Enzym dabei ist die Adipozyten-Triglycerid-Lipase (ATGL). Diese spaltet zunächst vom Triglycerid die erste Fettsäure ab.[7] Das dabei gebildete Diglycerid wird im zweiten Schritt von der Hormon-sensitiven Lipase (HSL) gespalten, wodurch wiederum eine Fettsäure, diesmal jedoch unter Bildung eines Monoglycerids freigesetzt wird. Im letzten Schritt spaltet die Monoglyceridlipase (MGL) das Monoglycerid und setzt die letzte Fettsäure und Glycerin frei. Die im Fettgewebe ebenfalls vorhandenen Cholesterin- und Retinylester werden von der HSL ebenfalls unter Freisetzung von Fettsäuren abgebaut.[8]
Die Steuerung der Lipolyse hängt eng mit der Regulation des Blutzuckerspiegels zusammen, da durch Glucagon einerseits der Fettabbau gesteigert, durch Insulin aber gehemmt wird. Die Ausschüttung von Adrenalin, Noradrenalin und anderen Phenylalkylaminen sowie Cortisol aktiviert die Lipolyse. Auch viele Arzneistoffe mit sogenannter sympathomimetischer Wirkung, d. h. stimulierender Wirkung auf das Vegetative Nervensystem, wirken auf den Fettabbau, wobei die Wirkung in den zwei verschiedenen Gruppen der Sympathomimetika entgegengesetzt ist (siehe Auflistung). Prostaglandine, Nicotinsäure und Betablocker hemmen die Lipolyse.
Aktivierung der Lipolyse erfolgt durch
Hemmung der Lipolyse erfolgt durch
In vielen Lebensmitteln wie Milch und Milchprodukten, Ölsaaten, Getreide, Obst und Gemüse sind sowohl Lipide, als auch die sie abbauenden Enzyme vorhanden. Daher läuft auch hier eine Lipolyse ab, die in den meisten Lebensmitteln unerwünscht ist. Bei der Käse- und Rohwurst-Herstellung sind diese Prozesse teilweise erwünscht. Es entstehen neben Mono- und Diestern des Glycerins auch kurz- und mittelkettige Fettsäuren, die Geschmack und Geruch des Lebensmittels negativ beeinflussen, etwa die übelriechende Buttersäure. Dieser Abbau wird als Fettverderb bezeichnet, wobei die entstehenden Fettsäuren bei Luftzutritt auch zu Lipidperoxiden oxidiert werden können. Beim Erhitzen von Lebensmitteln werden die Lipasen durch Denaturierung strukturell verändert und damit inaktiviert.[1] Diesen Vorgang nutzt man, um etwa Milch haltbar zu machen (Ultrahocherhitzung).