FAIR and interactive data graphics from a scientific knowledge graph
İçindekiler
| β-laktam antibiyotik | |
|---|---|
| İlaç sınıfı | |
 β-laktam antibiyotiklerin en yaygın 2 grubu olan penisilinlerin (üstte) ve sefalosporinlerin (altta) çekirdek yapısı. Kırmızı renkte beta-laktam halkası. | |
| Sınıf tanımlayıcıları | |
| Kullanım | Bakteriyel enfeksiyon |
| ATC kodu | J01C |
| Biyolojik hedef | Penisilin bağlayıcı proteinler |
| Dış bağlantılar | |
| MeSH | D047090 |
| Hukuki durum | |
| Vikiveri | |
β-laktam antibiyotikler (beta-laktam antibiyotikler) kimyasal yapılarında beta-laktam halkası içeren antibiyotiklerdir. Buna penisilin türevleri (penamlar), sefalosporinler ve sefamisinler (sefemler), monobaktamlar, karbapenemler[1] ve karbasepemler[2] dahildir. Çoğu β-laktam antibiyotik, bakteriyel organizmada hücre duvarı biyosentezini inhibe ederek çalışır ve en yaygın kullanılan antibiyotik grubudur. 2003 yılına kadar, satışlarla ölçüldüğünde, kullanımda olan ticari olarak mevcut tüm antibiyotiklerin yarısından fazlası β-laktam bileşikleriydi.[3] Keşfedilen ilk β-laktam antibiyotik olan penisilin, bir Penicillium rubens (o zamanki adıyla Penicillium notatum) türünden izole edilmiştir.[4][5]
Bakteriler genellikle β-laktam halkasına saldıran bir enzim olan β-laktamaz sentezleyerek β-laktam antibiyotiklere karşı direnç geliştirir. Bu direncin üstesinden gelmek için β-laktam antibiyotikler, klavulanik asit gibi β-laktamaz inhibitörleriyle birlikte verilebilir.[6]
Tıbbi kullanım
β-laktam antibiyotikler, duyarlı organizmaların neden olduğu bakteriyel enfeksiyonların önlenmesi ve tedavisi için endikedir. Başlangıçta β-laktam antibiyotikler yalnızca Gram-pozitif bakterilere karşı aktifken, son zamanlarda çeşitli Gram-negatif organizmalara karşı aktif olan geniş spektrumlu β-laktam antibiyotiklerin geliştirilmesi bu antibiyotiklerin kullanımını artırmıştır.[kaynak belirtilmeli]
İltihaplanmamış (normal) beyin zarlarında beta-laktam antibiyotiklerin penetrasyonu, AUCCSF/AUCS oranının (serebrosopinal sıvı eğrisi altındaki alanın serum eğrisi altındaki alana oranı) 0,15'i kadar düşüktür.[7]
Advers etkiler
Advers ilaç reaksiyonları
β-laktam antibiyotikler için yaygın advers ilaç reaksiyonları arasında ishal, bulantı, döküntü, ürtiker, süperenfeksiyon (kandidiyaz dahil) bulunur.[8]
Seyrek görülen advers etkiler arasında ateş, kusma, eritem, dermatit, anjiyoödem, psödomembranöz kolit sayılabilir.[8]
Enjeksiyon bölgesinde ağrı ve iltihaplanma, parenteral olarak uygulanan β-laktam antibiyotikler için de yaygındır.[kaynak belirtilmeli]
Alerji/aşırı duyarlılık
Herhangi bir β-laktam antibiyotiğe karşı immünolojik aracılı advers reaksiyonlar, bu ajanı alan hastaların %10'una kadarında meydana gelebilir (bunların küçük bir kısmı gerçekten IgE aracılı alerjik reaksiyonlardır, bkz. amoksisilin döküntüsü). Hastaların yaklaşık %0,01'inde anafilaksi meydana gelebilir.[8][9] Penisilin türevleri, sefalosporinler ve karbapenemler arasında belki de %5-10 oranında çapraz duyarlılık vardır;[kaynak belirtilmeli] ancak bu rakam çeşitli araştırmacılar[kim?] tarafından sorgulanmaktadır.[kaynak belirtilmeli]
Bununla birlikte, çapraz reaktivite riski, herhangi bir β-laktam antibiyotiğe karşı ciddi alerjik reaksiyon (ürtiker, anafilaksi, intersitisyel nefrit) öyküsü olan hastalarda tüm β-laktam antibiyotiklerin kontrendike olmasını gerektirecek düzeydedir. Nadiren, alerjik reaksiyonlar bu antibiyotikleri kullanan bir partnerle öpüşme ve cinsel temastan kaynaklanan maruziyetle tetiklenmiştir.[10]
Sifiliz gibi spiroketal bir enfeksiyonun bir β-laktam antibiyotik ile ilk tedavisinden sonra Jarisch-Herxheimer reaksiyonu meydana gelebilir.
Etki mekanizması
Hücre duvarı sentezinin engellenmesi
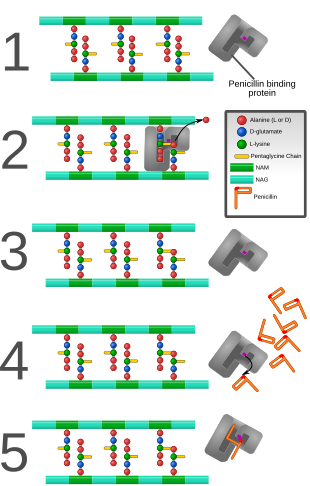
β-laktam antibiyotikler bakterisidaldir ve bakteriyel hücre duvarlarının peptidoglikan tabakasının sentezini inhibe ederek etki gösterirler. Peptidoglikan tabaka, özellikle Gram-pozitif organizmalarda, duvarın en dış ve birincil bileşeni olarak hücre duvarı yapısal bütünlüğü için önemlidir.[6] Peptidoglikan sentezindeki son transpeptidasyon adımı, penisilin bağlayıcı proteinler (PBP'ler) olarak da bilinen DD-transpeptidazlar tarafından kolaylaştırılır. PBP'ler penisilin ve diğer β-laktam antibiyotiklere olan afiniteleri bakımından farklılık gösterir. PBP'lerin sayısı bakteri türleri arasında değişiklik gösterir.[11]
β-laktam antibiyotikler, yeni oluşan peptidoglikan tabakasının öncü NAM/NAG-peptit alt birimlerindeki terminal amino asit kalıntıları olan D-alanil-D-alanin analoglarıdır. β-laktam antibiyotikler ile D-alanil-D-alanin arasındaki yapısal benzerlik, PBP'lerin aktif bölgesine bağlanmalarını kolaylaştırır. Molekülün β-laktam çekirdeği, PBP aktif bölgesinin Ser403 kalıntısına geri dönüşümsüz olarak bağlanır (asilatlar). PBP'lerin bu geri dönüşümsüz inhibisyonu, yeni oluşan peptidoglikan tabakasının nihai çapraz bağlanmasını (transpeptidasyon) önleyerek hücre duvarı sentezini bozar.[13]
β-laktam antibiyotikler sadece siyanobakteriler de dahil olmak üzere bakterilerin bölünmesini değil, aynı zamanda glokofitlerin fotosentetik organelleri olan siyanellerin bölünmesini ve briyofitlerin kloroplastlarının bölünmesini de engeller. Buna karşılık, oldukça gelişmiş damarlı bitkilerin plastitleri üzerinde hiçbir etkileri yoktur. Bu durum endosimbiyotik teoriyi desteklemekte ve kara bitkilerinde plastid bölünmesinin evrimine işaret etmektedir.[14]
Normal şartlar altında, peptidoglikan öncülleri bakteri hücre duvarının yeniden düzenlenmesine işaret eder ve sonuç olarak otolitik hücre duvarı hidrolazlarının aktivasyonunu tetikler. Çapraz bağlanmanın β-laktamlar tarafından engellenmesi, peptidoglikan öncüllerinin birikmesine neden olur ve bu da yeni peptidoglikan üretimi olmaksızın mevcut peptidoglikanın otolitik hidrolazlar tarafından sindirilmesini tetikler. Sonuç olarak, β-laktam antibiyotiklerin bakterisidal etkisi daha da artar.[kaynak belirtilmeli]
Guanin oksidasyonu
Beta laktamların sitotoksisitesinin çoğunu açıklamak için önerilen bir başka olasılık, bakteriyel nükleotid havuzundaki guanin nükleotidinin oksidasyonuna odaklanmaktadır.[15] Oksitlenmiş guanin nükleotidinin DNA'ya dahil olması sitotoksisiteye neden olabilir. Bakteriyel sitotoksisite, DNA'daki yakın aralıklı 8-okso-2'-deoksiguanozin lezyonlarının eksik onarımından kaynaklanabilir ve bu da çift iplikçik kırılmalarına neden olabilir.[15]
Potens
β-laktam antibiyotiklerin iki yapısal özelliği antibiyotik potensleri ile ilişkilendirilmiştir.[16] Bunlardan ilki "Woodward parametresi" olarak bilinen h'dir ve β-laktamın tepe noktası olarak nitrojen atomu ve taban olarak üç komşu karbon atomu tarafından oluşturulan piramidin yüksekliğidir (angstrom cinsinden).[17] İkincisi "Cohen parametresi" olarak adlandırılır, c ve karboksilatın karbon atomu ile β-laktam karbonilinin oksijen atomu arasındaki mesafedir.[18] Bu mesafenin, karboksilat bağlama bölgesi ile PBP enziminin oksiyanyon deliği arasındaki mesafeye karşılık geldiği düşünülmektedir. En iyi antibiyotikler daha yüksek h değerlerine (hidrolize karşı daha reaktif) ve daha düşük c değerlerine (PBP'lere daha iyi bağlanma) sahip olanlardır.[16]
Direnç biçimleri
Tanım gereği, tüm β-laktam antibiyotiklerin yapısında bir β-laktam halkası bulunur. Bu antibiyotiklerin etkinliği, PBP'ye bozulmadan ulaşma ve PBP'ye bağlanma kabiliyetlerine dayanır. Bu nedenle, β-laktamlara karşı bakteriyel direncin iki ana modu vardır:
β-laktam halkasının enzimatik hidrolizi
Bakteri β-laktamaz enzimi veya penisilinaz enzimi üretirse, enzim antibiyotiğin β-laktam halkasını hidrolize ederek antibiyotiği etkisiz hale getirecektir. (Bu tür bir enzime örnek olarak 2009 yılında keşfedilen Yeni Delhi metallo-beta-laktamaz 1 verilebilir).[19] Bu enzimleri kodlayan genler bakteriyel kromozomda doğal olarak mevcut olabilir veya plazmid transferi (plazmid aracılı direnç) yoluyla edinilebilir ve β-laktamaz gen ekspresyonu β-laktamlara maruz kalma ile indüklenebilir.[kaynak belirtilmeli]


Bir bakteri tarafından β-laktamaz üretilmesi, β-laktam antibiyotiklerle tüm tedavi seçeneklerini ortadan kaldırmaz. Bazı durumlarda, β-laktam antibiyotikler bir β-laktamaz inhibitörü ile birlikte uygulanabilir. Örneğin, Augmentin (FGP) amoksisilin (bir β-laktam antibiyotik) ve klavulanik asitten (bir β-laktamaz inhibitörü) oluşur. Klavulanik asit, tüm β-laktamaz enzimlerini bastırmak ve amoksisilinin β-laktamaz enzimlerinden etkilenmemesi için etkili bir antagonist görevi görmek üzere tasarlanmıştır. Bir diğer β-laktam/β-laktamaz inhibitörü kombinasyonu, Gram-pozitif ve negatif aerobik ve anaerobik bakterileri içeren geniş bir antibakteriyel aktivite spektrumuna sahip piperasilin/tazobaktamdır. Piperasiline tazobaktam eklenmesi, bazı geniş spektrumlu β-laktamazlar da dahil olmak üzere çok çeşitli β-laktamaz enzimlerine karşı stabilitesini artırmıştır.[20]
Boronik asitler gibi diğer β-laktamaz inhibitörleri, β-laktamazların aktif bölgesine geri dönüşümsüz olarak bağlandıkları için üzerinde çalışılmaktadır. Bu, klavulanik asit ve benzeri beta-laktam rakiplerine göre bir avantajdır, çünkü hidrolize edilemezler. Şu anda beta-laktamazların farklı izozimlerini hedeflemek üzere özel boronik asitler geliştirmek için kapsamlı araştırmalar yapılmaktadır.[21]
Bununla birlikte, β-laktamaz üreten bakterilerle enfeksiyondan şüphelenilen tüm durumlarda, tedavi öncesinde uygun bir β-laktam antibiyotik seçimi dikkatle değerlendirilmelidir. Özellikle, uygun β-laktam antibiyotik tedavisinin seçilmesi, belirli düzeyde β-laktamaz ekspresyonu barındıran organizmalara karşı büyük önem taşımaktadır. Bu durumda, tedavinin başlangıcında en uygun β-laktam antibiyotik tedavisinin kullanılmaması, daha yüksek düzeyde β-laktamaz ekspresyonuna sahip bakterilerin seçilmesine neden olabilir ve böylece diğer β-laktam antibiyotiklerle daha fazla çaba gösterilmesini zorlaştırabilir.[22]
Değiştirilmiş penisilin bağlayıcı proteinlere sahip olma
Bakteriyel enfeksiyonları kontrol etmek için β-laktamların kullanımına bir yanıt olarak, bazı bakteriler yeni yapılara sahip penisilin bağlayıcı proteinler geliştirmiştir. β-laktam antibiyotikler bu değiştirilmiş PBP'lere etkili bir şekilde bağlanamaz ve sonuç olarak β-laktamlar hücre duvarı sentezini bozmada daha az etkilidir. Bu direnç modunun dikkate değer örnekleri arasında metisiline dirençli Staphylococcus aureus (MDSA)[23] ve penisiline dirençli Streptococcus pneumoniae yer almaktadır. Değişmiş PBP'ler, β-laktam antibiyotiklerle tüm tedavi seçeneklerini ortadan kaldırmaz.
Adlandırma
β-laktamlar çekirdek halka yapılarına göre sınıflandırılır.[24]
- Doymuş beş üyeli halkalara kaynaşmış β-laktamlar:
- Tiyazolidin halkaları içeren β-laktamlar penam olarak adlandırılır.
- Pirolidin halkaları içeren β-laktamlar karbapenamlar olarak adlandırılır.
- Oksazolidin halkalarına kaynaşmış β-laktamlar oksapenamlar veya klavamlar olarak adlandırılır.
- Doymamış beş üyeli halkalara kaynaşmış β-laktamlar:
- 2,3-dihidrotiyazol halkaları içeren β-laktamlar penem olarak adlandırılır.
- 2,3-dihidro-1H-pirol halkaları içeren β-laktamlar karbapenem olarak adlandırılır.
- Doymamış altı üyeli halkalara kaynaşmış β-laktamlar:
- 3,6-dihidro-2H-1,3-tiyazin halkaları içeren β-laktamlar sefem olarak adlandırılır.
- 1,2,3,4-tetrahidropiridin halkaları içeren β-laktamlar karbasefem olarak adlandırılır.
- 3,6-dihidro-2H-1,3-oksazin halkaları içeren β-laktamlar oksasefem olarak adlandırılır.
- Başka bir halkaya kaynaşmamış β-laktamlar monobaktam olarak adlandırılır.
Geleneksel olarak, bisiklik β-laktamlar, belirli bir sınıfta hangi atom olduğuna bakılmaksızın, penam ve sefemlerde sülfürün işgal ettiği konumdan başlayarak numaralandırılır. Yani, pozisyon 1 her zaman β-laktam halkasının β-karbonuna bitişiktir. Numaralandırma, β-laktamın β-karbonuna ulaşılana kadar birinci konumdan saat yönünde devam eder ve bu noktada numaralandırma, kalan karbonları numaralandırmak için laktam halkası etrafında saat yönünün tersine devam eder. Örneğin, beş üyeli halkalara kaynaşmış tüm bisiklik β-laktamların azot atomu, penamlarda olduğu gibi 4. pozisyonda etiketlenirken, sefemlerde azot 5. pozisyondadır.
Monobaktamların numaralandırılması IUPAC'a uygundur; nitrojen atomu 1, karbonil karbonu 2, α-karbonu 3 ve β-karbonu 4 konumundadır.
Biyosentez
Bugüne kadar, bu antibiyotik ailesinin β-laktam çekirdeğini biyosentezlemek için iki farklı yöntem keşfedilmiştir. Keşfedilen ilk yol, penam ve sefemlerin yoludur. Bu yol, lineer tripeptit δ-(L-α-aminoadipil)-L-sistein-D-valin (ACV) üreten bir nonribozomal peptit sentetaz (NRPS), ACV sentetaz (ACVS) ile başlar. ACV, penam çekirdek yapısını oluşturmak için izopenisilin N sentaz (IPNS) tarafından bisiklik ara ürün izopenisilin N'ye oksidatif olarak siklize edilir (tek bir enzimle iki siklizasyon).[25] Çeşitli transamidasyonlar farklı doğal penisilinlere yol açar.
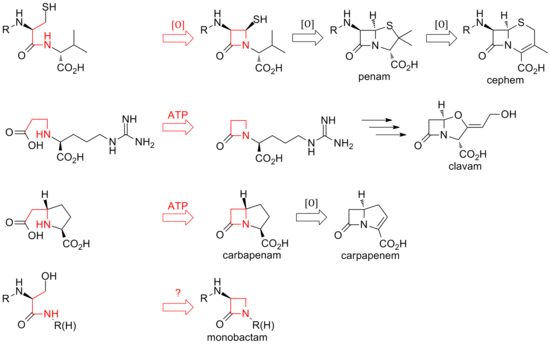
Sefemlerin biyosentezi, izopenisilin N'de oksidatif bir halka genişlemesi ile sefem çekirdeğine dallanır. Penisilinlerde olduğu gibi, sefalosporinler ve sefamisinlerin çeşitliliği de farklı transamidasyonlardan kaynaklanır.
Penam ve sefemlerde halka kapanması β-laktamın 1. ve 4. pozisyonları arasında ve oksidatif olarak gerçekleşirken, klavam ve karbapenemlerin halkaları halkanın 1. ve 2. pozisyonları arasında iki elektronlu süreçlerle kapanır. Bu siklizasyonlardan β-laktam sentetazlar sorumludur ve açık halka substratlarının karboksilatı ATP tarafından aktive edilir.[26] Klavamlarda β-laktam ikinci halkadan önce oluşur; karbapenemlerde ise β-laktam halkası ikinci sırada kapanır.[kaynak belirtilmeli]
Tabtoksinin β-laktam halkasının biyosentezi, klavamlar ve karbapenemlerinkini yansıtmaktadır. Sulfazecin ve nocardicinler gibi diğer monobaktamlarda laktam halkasının kapanması, β-karbonunda konfigürasyonun ters çevrilmesini içeren üçüncü bir mekanizmayı içerebilir.[27]
Ayrıca bakınız
Kaynakça
- ^ Holten KB, Onusko EM (August 2000). "Appropriate prescribing of oral beta-lactam antibiotics". American Family Physician. 62 (3). ss. 611-20. PMID 10950216. 6 Haziran 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Kasım 2008.
- ^ Yao, JDC; Moellering, RC Jr. (2007). "Antibacterial agents". Murray, PR (Ed.). Manual of Clinical Microbiology. 9th. Washington D.C.: ASM Press. Cited in Non-Penicillin Beta Lactam Drugs: A CGMP Framework for Preventing Cross-Contamination. U.S. Department of Health and Human Services; Food and Drug Administration; Center for Drug Evaluation and Research (CDER). April 2013. 13 Aralık 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Mayıs 2019 – US FDA website vasıtasıyla.
- ^ Elander, R. P. (2003). "Industrial production of β-lactam antibiotics". Applied Microbiology and Biotechnology. 61 (5–6). ss. 385-392. doi:10.1007/s00253-003-1274-y. PMID 12679848.
- ^ Houbraken, Jos; Frisvad, Jens C.; Samson, Robert A. (2011). "Fleming's penicillin producing strain is not Penicillium chrysogenum but P. rubens". IMA Fungus (İngilizce). 2 (1). ss. 87-95. doi:10.5598/imafungus.2011.02.01.12. PMC 3317369 $2. PMID 22679592.
- ^ Pathak A, Nowell RW, Wilson CG, Ryan MJ, Barraclough TG (September 2020). "Comparative genomics of Alexander Fleming's original Penicillium isolate (IMI 15378) reveals sequence divergence of penicillin synthesis genes". Scientific Reports. 10 (1). ss. Article 15705. Bibcode:2020NatSR..1015705P. doi:10.1038/s41598-020-72584-5. PMC 7515868 $2. PMID 32973216.
- ^ a b Pandey, N.; Cascella, M. (2020). "Beta lactam antibiotics". StatPearls. PMID 31424895. 15 Aralık 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2020.
- ^ Nau R, Sörgel F, Eiffert H (October 2010). "Penetration of drugs through the blood-cerebrospinal fluid/blood-brain barrier for treatment of central nervous system infections". Clinical Microbiology Reviews. 23 (4). ss. 858-83. doi:10.1128/CMR.00007-10. PMC 2952976 $2. PMID 20930076.
- ^ a b c Rossi S (ed.) (2004). Australian Medicines Handbook 2004. Adelaide: Australian Medicines Handbook. 0-9578521-4-2.
- ^ Pichichero ME (April 2005). "A review of evidence supporting the American Academy of Pediatrics recommendation for prescribing cephalosporin antibiotics for penicillin-allergic patients". Pediatrics. 115 (4). ss. 1048-57. doi:10.1542/peds.2004-1276. PMID 15805383.
- ^ Liccardi, Gennaro; Caminati, Marco; Senna, Gianenrico; Calzetta, Luigino; Rogliani, Paola (October 2017). "Anaphylaxis and intimate behaviour". Current Opinion in Allergy and Clinical Immunology. 17 (5). ss. 350-355. doi:10.1097/ACI.0000000000000386. ISSN 1473-6322. PMID 28742538. 25 Nisan 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Şubat 2021.
- ^ a b Miyachiro, M. M.; Contreras-Martel, C.; Dessen, A. (2019). "Penicillin-Binding Proteins (PBPS) and Bacterial Cell Wall Elongation Complexes". Macromolecular Protein Complexes II: Structure and Function. Subcellular Biochemistry. 93. ss. 273-289. doi:10.1007/978-3-030-28151-9_8. ISBN 978-3-030-28150-2. PMID 31939154.
- ^ Cushnie, T. P.; O'Driscoll, N. H.; Lamb, A. J. (2016). "Morphological and ultrastructural changes in bacterial cells as an indicator of antibacterial mechanism of action". Cellular and Molecular Life Sciences. 73 (23). ss. 4471-4492. doi:10.1007/s00018-016-2302-2. hdl:10059/2129. PMID 27392605. 7 Ekim 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2020.
- ^ Fisher, J. F.; Meroueh, S. O.; Mobashery, S. (2005). "Bacterial resistance to β-lactam antibiotics: compelling opportunism, compelling opportunity". Chemical Reviews. 105 (2). ss. 395-424. doi:10.1021/cr030102i. PMID 15700950.
- ^ Kasten, B.; Reski, R. (1 Ocak 1997). "β-Lactam antibiotics inhibit chloroplast division in a moss (Physcomitrella patens) but not in tomato (Lycopersicon esculentum)". Journal of Plant Physiology. 150 (1). ss. 137-140. doi:10.1016/S0176-1617(97)80193-9.
- ^ a b Foti, James J.; Devadoss, Babho; Winkler, Jonathan A.; Collins, James J.; Walker, Graham C. (20 Nisan 2012). "Oxidation of the guanine nucleotide pool underlies cell death by bactericidal antibiotics". Science. 336 (6079). ss. 315-319. Bibcode:2012Sci...336..315F. doi:10.1126/science.1219192. PMC 3357493 $2. PMID 22517853.
- ^ a b Nangia, Ashwini; Biradha, Kumar; Desiraju, Gautam R. (1996). "Correlation of biological activity in β-lactam antibiotics with Woodward and Cohen structural parameters—a Cambridge database study". Journal of the Chemical Society, Perkin Transactions 2, 5. ss. 943-953. doi:10.1039/p29960000943. ISSN 1364-5471.
- ^ Woodward, R. B. (16 Mayıs 1980). "Penems and related substances". Philosophical Transactions of the Royal Society of London B: Biological Sciences. 289 (1036). ss. 239-250. Bibcode:1980RSPTB.289..239W. doi:10.1098/rstb.1980.0042. ISSN 0962-8436. PMID 6109320.
- ^ Cohen, N. Claude (1 Şubat 1983). ".beta.-Lactam antibiotics: geometrical requirements for antibacterial activities". Journal of Medicinal Chemistry. 26 (2). ss. 259-264. doi:10.1021/jm00356a027. ISSN 0022-2623. PMID 6827544.
- ^ Drawz, S. M.; Bonomo, R. A. (2010). "Three decades of β-lactamase inhibitors". Clinical Microbiology Reviews. 23 (1). ss. 160-201. doi:10.1128/CMR.00037-09. PMC 2806661 $2. PMID 20065329.
- ^ Gin, Alfred; Dilay, Leanne; Karlowsky, James A; Walkty, Andrew; Rubinstein, Ethan; Zhanel, George G (June 2007). "Piperacillin–tazobactam: a β-lactam/β-lactamase inhibitor combination". Expert Review of Anti-infective Therapy (İngilizce). 5 (3). ss. 365-383. doi:10.1586/14787210.5.3.365. ISSN 1478-7210. PMID 17547502.
- ^ Leonard, David A.; Bonomo, Robert A.; Powers, Rachel A. (19 Kasım 2013). "Class D β-Lactamases: a reappraisal after five decades". Accounts of Chemical Research. 46 (11). ss. 2407-2415. doi:10.1021/ar300327a. ISSN 0001-4842. PMC 4018812 $2. PMID 23902256.
- ^ Macdougall C (2011). "Beyond susceptible and resistant Part I: treatment of infections due to Gram-negative organisms with inducible B-lactamases". Journal of Pediatric Pharmacology and Therapeutics. 16 (1). ss. 23-30. doi:10.5863/1551-6776-16.1.23. PMC 3136230 $2. PMID 22477821.
- ^ Ubukata, K.; Nonoguchi, R.; Matsuhashi, M.; Konno, M. (1989). "Expression and inducibility in Staphylococcus aureus of the mecA gene, which encodes a methicillin-resistant S. aureus-specific penicillin-binding protein". Journal of Bacteriology. 171 (5). ss. 2882-5. doi:10.1128/jb.171.5.2882-2885.1989. PMC 209980 $2. PMID 2708325.
- ^ Dalhoff, A.; Janjic, N.; Echols, R. (2006). "Redefining penems". Biochemical Pharmacology. 71 (7). ss. 1085-1095. doi:10.1016/j.bcp.2005.12.003. PMID 16413506.
- ^ Lundberg, M.; Siegbahn, P. E. M.; Morokuma, K. (2008). "The mechanism for isopenicillin N synthase from density-functional modeling highlights the similarities with other enzymes in the 2-His-1-carboxylate family". Biochemistry. 47 (3). ss. 1031-1042. doi:10.1021/bi701577q. PMID 18163649. 22 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Ekim 2017.
- ^ Bachmann, B. O.; Li, R.; Townsend, C. A. (1998). "β-lactam synthetase: a new biosynthetic enzyme". Proceedings of the National Academy of Sciences of the United States of America. 95 (16). ss. 9082-9086. Bibcode:1998PNAS...95.9082B. doi:10.1073/pnas.95.16.9082. PMC 21295 $2. PMID 9689037.
- ^ Townsend, CA; Brown, AM; Nguyen, LT (1983). "Nocardicin A: stereochemical and biomimetic studies of monocyclic β-lactam formation". Journal of the American Chemical Society. 105 (4). ss. 919-927. doi:10.1021/ja00342a047.



















