Effects of the storage conditions on the stability of natural and synthetic cannabis in biological matrices for forensic toxicology analysis: An update from the literature
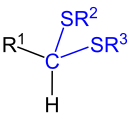
Thioacetale sind chemische Verbindungen, die sich von Aldehyden ableiten und statt der Carbonylgruppe (a) zwei Sulfanyl-Gruppen (–SR1 und –SR2) oder (b) je eine Sulfanyl-Gruppe (–SR1) und eine Alkoxygruppe oder Aryloxygruppe (–OR2) enthalten, die an dasselbe Kohlenstoff-Atom gebunden sind. Sie sind geminal angeordnete Schwefelanaloga von Diethern.
Ursprünglich wurde zwischen den aus Aldehyden gebildeten Thioacetalen (mit einem H-Atom) und den aus Ketonen gebildeten analogen Verbindungen, den so genannten Thioketalen, unterschieden. Heutzutage werden auch Thioketale meist als Unterklasse der Thioacetale betrachtet.
Bei der Bildung von Thioacetalen aus Aldehyden bzw. Ketonen und Thiolen entstehen als Zwischenprodukte die Hemi- bzw. Monothiohalbacetale [R'2C(SR)(OH)][1], welche nur in einigen Fällen isoliert werden können.
Synthese
Dithioacetale bilden sich bei der Umsetzung von Aldehyden (Beispiel: Acetaldehyd) und ein- oder zweiwertigen Thiolen (Beispiel: 1,3-Propandithiol) unter Wasserabspaltung. In der Regel wird diese Kondensationsreaktion unter Säurekatalyse durchgeführt.
Dithioacetale als Schutzgruppen
In der Synthesechemie werden Dithioacetale oft als Schutzgruppen für Carbonylgruppen von Aldehyden oder Ketonen benutzt.
In der Corey-Seebach-Reaktion dienen Dithioacetale als Zwischenprodukte zur Synthese von unsymmetrischen Ketonen aus Aldehyden.
Verwandte Verbindungen
S,N-Acetale
Wenn die Carbonylgruppe eines Aldehyds oder eines Ketons mit einem 1,2-Aminothiol unter Wasserabspaltung umgesetzt wird, entsteht ein S,N-Acetal. Thiazolidine und 3-Thiazoline sind Beispiele für heterocyclische S,N-Acetale.
Einzelnachweise
- ↑ Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 6: T–Z. 8. neubearbeitete und erweiterte Auflage. Franckh’sche Verlagshandlung, Stuttgart 1988, ISBN 3-440-04516-1, S. 4236.