Effects of the storage conditions on the stability of natural and synthetic cannabis in biological matrices for forensic toxicology analysis: An update from the literature
Die Stephen-Aldehyd-Synthese ist eine Reaktion der organischen Chemie, bei der es sich um die Synthese von Aldehyden aus Nitrilen handelt.[1] Die Reaktion wurde zuerst von Henry Stephen 1925 erwähnt.[1]
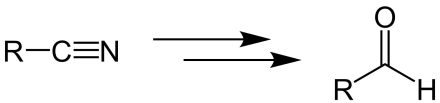
Übersichtsreaktion
Bei dieser Synthese werden die Nitrile mit Zinn(II)-chlorid behandelt, um kristallines Aldimin-Zinnchlorid zu erhalten, welches dann hydrolysiert wird.
Reaktionsmechanismus
Im Folgenden wird der postulierte Reaktionsablauf erklärt:

Durch Zugabe von Chlorwasserstoff reagiert das Nitril (1) in Ether zum korrespondierenden Salz (2). Es wird angenommen, dass dieses Salz durch eine Einelektronenübertragung vom Zinn(II)-chlorid reduziert wird (3a und 3b).[1] Das entstandene Salz (4) fällt nach einiger Zeit als Aldimin-Zinnchlorid (5) aus. Durch Hydrolyse von 5 entsteht ein Carbonsäureamid (6) aus welchem dann ein Aldehyd (7) entsteht.
Substituenten, die die Elektronendichte erhöhen, begünstigen die Bildung des Aldimin-Zinnchlorid-Addukts. Durch elektronenziehende Substituenten wird die Bildung des Amidchlorids erleichtert.[2] Früher lag der Erfolg der Reaktion darin, dass das Aldimin-Zinnchlorid ausgefallen ist, mit Ether gewaschen und anschließend hydrolysiert wurde.[1] Es wurde jedoch herausgefunden, dass es nicht notwendig ist das Aldimin-Zinnchlorid aus der Lösung zu entfernen. Das Präparat kann direkt in der Lösung hydrolysiert werden.[1]
Diese Reaktion ist ertragreicher, wenn aromatische Nitrile anstatt aliphatischer Nitrile verwendet werden. Aber auch bei einigen aromatischen Nitrilen ist die Ausbeute gering (z. B. 2-Formylbenzoesäureethylester).[1]
Einzelnachweise
- ↑ a b c d e f Zerong Wang: Comprehensive Organic Name Reactions and Reagents, 3 Volume Set. John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 2659–2660.
- ↑ M. Rabinovitz: The Cyano Group (1970). John Wiley & Sons, Chichester, UK 1970, ISBN 0-470-77124-0, S. 308. doi:10.1002/9780470771242.ch7












